Пародонтит, как известно, вызывается неадекватной активацией ответа организма хозяина на рост биоплёнок, что приводит к дисбиозу, то есть нарушению состава и функций микробного сообщества. Исторические гипотезы о зубной бляшке дают базовое понимание ее роли в патогенезе пародонтита. Современные теории показывают, как дисбиоз может запускать чрезмерную реакцию иммунной системы, приводящую к разрушению тканей и развитию пародонтита.
В сложной экосистеме человеческого организма разнообразные микроорганизмы обитают в различных анатомических зонах, включая кожу, дыхательные пути, мочеполовую и желудочно-кишечную системы, в том числе и полость рта. Эти микроорганизмы, в совокупности называемые микробиотой, играют ключевую роль в поддержании здоровья благодаря взаимодействию с иммунной системой.
Оральная микробиота составляет значительную часть человеческой микробиоты и включает более 700 различных видов, в том числе бактерии, грибы, вирусы и простейшие. Полость рта содержит второе по разнообразию микробное сообщество в организме человека.
Эти микроорганизмы заселяют определённые микроокружения в полости рта, такие как зубы, десневой желобок, язык, твёрдое и мягкое нёбо, а также миндалины. Каждая из этих ниш имеет уникальную локальную среду, определяющую состав и поведение микробных сообществ, позволяя им существовать либо в планктонной форме, либо в составе сложных полимикробных биоплёнок.
В норме между оральной микробиотой и хозяином существует симбиотическая связь, при которой обе стороны получают пользу от этого взаимодействия. Сбалансированная и разнообразная микробиота обеспечивает защиту от инфекций и помогает поддерживать гомеостаз. Нарушение этого баланса, приводящее к дисбиозу, может иметь серьёзные последствия.
Дисбиоз возникает при снижении количества полезных микробов или увеличении числа патогенных микроорганизмов, что приводит к нарушению микробного равновесия и запускает неадекватную активацию защитных механизмов организма.
Такой дисбаланс между оральным микробиомом и иммунной системой хозяина связан с развитием пародонтита, а также с рядом системных заболеваний, включая сердечно-сосудистые заболевания, сахарный диабет, болезнь Альцгеймера, онкологические заболевания, ревматоидный артрит, хроническую болезнь почек, воспалительные заболевания кишечника и болезни дыхательной системы.
Взаимодействие между хозяином и оральной микробиотой внутри дентальных биопленок играет решающую роль в переходе от пародонтального здоровья к пародонтальной патологии. Поэтому цели данного обзора заключаются в следующем: предоставить актуальную информацию о роли биопленки в этиологии пародонтита и рассмотреть исторические и современные гипотезы, предложенные для объяснения патогенеза пародонтита.
Дентальная биопленка
Дентальная биопленка, часто называемая зубной бляшкой, представляет собой стойкий слой, состоящий из разнообразных микроорганизмов в матриксе внеклеточных полимеров. Она формируется непрерывно и естественным образом на поверхностях в полости рта, включая зубы, дентальные имплантаты и протезы.
Микроорганизмы составляют около 70% сухого веса биоплёнки, остальная часть представлена матриксом из полисахаридов, слюнных белков и гликопротеинов. Матрикс в составе биоплёнки выполняет несколько функций: обеспечивает защиту, способствует прикреплению микроорганизмов к поверхностям, поддерживает структурную стабильность биоплёнки и поставляет питательные вещества, необходимые для роста и выживания микробов.
Процесс образования биопленки приносит пользу хозяину, защищая от экзогенной колонизации патогенными бактериями. Формирование биоплёнки создаёт микробную среду, которая препятствует прикреплению патогенных бактерий к поверхности зубов и их доступу к питательным веществам, тем самым снижая вероятность инфекций. Кроме того, хорошо сформированная биоплёнка помогает поддерживать сбалансированное микробное сообщество, играющее роль в предотвращении избыточного роста патогенов.
Однако при отсутствии регулярного разрушения растущей биопленки с помощью надлежащей гигиены полости рта может развиться гингивит – это воспалительное состояние, характеризующееся гиперемией и отёком десны без утраты прикрепления.
Развитие гингивита, вызванного зубным налётом, было продемонстрировано в знаковом экспериментальном исследовании гингивита, где у участников, отказавшихся от гигиены полости рта, предсказуемо развился гингивит.
Таким образом, дентальная биопленка признана основным этиологическим фактором развития воспаления в тканях десны, которое у предрасположенных индивидов может прогрессировать в пародонтит.
Формирование биоплёнки начинается с образования пелликулы — тонкой плёнки, состоящей из слюнных гликопротеинов и десневой жидкости, которая прикрепляется к поверхности зуба посредством случайных или химических взаимодействий. Первичное прикрепление происходит между бактериальными клетками и пелликулой, что приводит к формированию плотно прилегающей полосы микроорганизмов на эмали или поверхности корня. Это прикрепление включает обратимые, слабые, дальнодействующие физико-химические взаимодействия.
Первичную колонизацию пелликулы осуществляют преимущественно грамотположительные аэробные кокки и палочки, такие как стрептококки и актиномицеты, которые ассоциируются с пародонтальным здоровьем. По мере закрепления этих ранних колонизаторов они способствуют последующему прикреплению промежуточных и поздних колонизаторов — грамотрицательных анаэробов, таких как Fusobacterium nucleatum, Porphyromonas gingivalis, Tannerella forsythia, Treponema denticola и Aggregatibacter actinomycetemcomitans.
Адгезионные свойства этих бактерий включают взаимодействие между бактериальными адгезинами и рецепторами хозяина, что имеет решающее значение для бактериальной преемственности внутри агрегата биоплёнки; поздние колонизаторы в конечном счёте заменяют ранних, способствуя созреванию биопленки.
По мере созревания биопленки она становится более структурированной, с формированием различных микробных сообществ и повышенной устойчивостью к деструкции и антимикробным агентам. Этот процесс созревания имеет ключевое значение для способности биоплёнки вызывать заболевание.
Патогенные микроорганизмы могут размножаться внутри биоплёнки, избегая иммунных ответов организма за счёт особых факторов вирулентности. Кроме того, микроорганизмы в составе биоплёнки обладают большей устойчивостью к уничтожению по сравнению со своими свободноплавающими аналогами благодаря защитному матриксу и кооперативным взаимодействиям, что позволяет им уклоняться от действия иммунной системы и антимикробных препаратов.
Таким образом, использование системных антимикробных препаратов в качестве единственного метода лечения пародонтита противопоказано. Они должны применяться только в сочетании с механическим разрушением биоплёнки путём профессионального удаления зубного налёта.
Исторические гипотезы о роли биопленки
Гипотеза неспецифической бляшки
В 1890 году Миллер предложил гипотезу неспецифической бляшки (NSPH — Non-Specific Plaque Hypothesis), которая установила связь между зубной бляшкой и развитием заболеваний пародонта. Согласно NSPH, заболевание пародонта возникает вследствие общей микробной массы бляшки, а не из-за какого-либо конкретного микроорганизма или его вирулентности.
В частности, эта гипотеза утверждает, что все бактерии в составе биоплёнки обладают равным потенциалом вызывать заболевание, а реакция организма на бляшку пропорциональна её количеству, независимо от вирулентности отдельных бактерий.
Сильной стороной NSPH является акцент на коллективное действие всей микробной массы бляшки, что упрощает понимание механизмов заболевания путём отнесения их к общей микробной нагрузке.
Такой подход поддерживает прямолинейные профилактические меры, например, тщательное удаление налёта за счёт хорошей гигиены полости рта. Однако NSPH не учитывает специфическую роль отдельных видов бактерий в прогрессировании заболевания, что может привести к чрезмерно обобщённым стратегиям лечения.
Гипотеза специфической бляшки
Гипотеза специфической бляшки (SPH — Specific Plaque Hypothesis), предложенная Лёше в 1976 году, акцентировала внимание на идентификации конкретных микроорганизмов, связанных с заболеванием пародонта, и различии между микробиомом при здоровье и при болезни.
Согласно SPH, переход от здорового состояния бляшки к патологическому связан с появлением определённых поддесневых бактерий с высокой вирулентностью, способствующих прогрессированию заболевания.
Ключевой особенностью SPH является идентификация специфических патогенных бактерий, ответственных за пародонтит, что способствует более целенаправленному диагностическому и терапевтическому подходу.
Однако эффективное воздействие на конкретные микроорганизмы остаётся ограниченным, а потенциальная роль вакцинации против специфических патогенов требует проведения масштабных исследований.
Основным недостатком гипотезы специфической бляшки (SPH) является то, что она не учитывает случаи, когда у отдельных людей наблюдается значительное накопление зубного налёта, но при этом не развивается тяжёлый пародонтит. SPH рассматривает заболевание пародонта как инфекцию, вызванную специфическими патогенными микроорганизмами, при этом тяжесть заболевания связывается с наличием или увеличением количества этих конкретных микробов, а не с нарушенной реакцией со стороны организма.
Экологическая теория
Гипотеза экологического сдвига, предложенная Маршем в 1994 году, предполагает, что изменения в составе и количестве оральной микробиоты в биоплёнке способствуют переходу от здоровья к заболеванию.
Согласно этой гипотезе, изменения в разнообразии и численности микробов происходят под воздействием экологических стрессоров, включая факторы, связанные с хозяином (например, иммунодефицитные состояния, беременность и другие), и факторы окружающей среды (такие как курение, диета и другие).
Эти стрессоры приводят к хроническому воспалению и разрушению тканей, создавая среду, благоприятную для формирования дисбиотических микробных сообществ. В результате наблюдается снижение количества комменсальных (нормальных) видов и увеличение числа потенциально патогенных видов в составе биоплёнки.
Сильной стороной гипотезы экологического сдвига является её акцент на то, как иммунный ответ хозяина и изменения окружающей среды в полости рта, например, уровень pH и доступность питательных веществ, влияют на состав микробиоты. Такой взгляд обеспечивает более целостное понимание этиологии заболевания и поддерживает подходы к лечению, направленные на восстановление микробного баланса в полости рта.
Однако динамический характер микробных экосистем может затруднять разработку прямолинейных протоколов лечения, поскольку изменения микробных сообществ определяются сложным взаимодействием множества факторов.
Современные концепции
Модель ключевого патогена
Модель ключевого патогена, предложенная Хаджисенгалисом и соавторами в 2012 году, описывает, как определённые микробные виды, несмотря на их низкую численность, могут оказывать несоразмерно сильное воздействие на окружающую микробную среду.
Согласно этой модели, ключевые патогены нарушают иммунный ответ хозяина и инициируют воспалительные заболевания путём дестабилизации симбиотической микробиоты, что приводит к дисбиозу. Хотя сами по себе эти патогены недостаточны для развития заболевания, они вызывают патогенные изменения в микробиоте за счёт модификации её состава, способствуя тем самым развитию болезни.
Модель подчёркивает важную роль взаимодействия между ключевыми патогенами и комменсальной микробиотой. Например, Porphyromonas gingivalis идентифицирована как основной ключевой патоген, который способен избегать защитных механизмов хозяина и способствовать формированию патогенной, дисбиотической биоплёнки. Это взаимодействие имеет решающее значение как для уклонения от иммунного ответа, так и для поддержания воспаления.
Главное преимущество модели ключевого патогена заключается в её потенциале для разработки целенаправленных терапевтических стратегий, ориентированных на определённые ключевые микроорганизмы, а также в углублении понимания механизмов развития заболевания.
Однако её узкая направленность на отдельные патогены может не учитывать более широкие взаимодействия между различными микробными видами и факторами окружающей среды, которые также вносят вклад в прогрессирование заболевания.
Модель полимикробной синергии и дисбиоза
Модель полимикробной синергии и дисбиоза (PSD — Polymicrobial Synergy and Dysbiosis) при пародонтите, предложенная Ламонтом и Хаджисенгалисом в 2015 году, ставит под сомнение традиционное представление о том, что пародонтит вызывается конкретными пародонтопатогенными микроорганизмами.
Вместо этого она приписывает развитие пародонтита дисбиотической, синергичной микробиоте.
Модель подчёркивает кооперативные взаимодействия между множеством микробных видов, которые способствуют развитию дисбиоза и заболевания, предлагая целостный взгляд на патогенез. Пародонтит рассматривается как результат самоподдерживающегося цикла дисбиоза и воспалительной резорбции кости, приводящего к повреждению тканей.
Модель PSD также подчёркивает роль ключевых патогенов с взаимно усиливающимися факторами вирулентности, которые способствуют формированию микробного сообщества, обладающего полимикробной синергией. Эта синергия позволяет таким патогенам уклоняться от иммунного ответа хозяина и усиливать воспаление, способствуя прогрессированию пародонтита.
Подчёркивая эти сложные микробные взаимодействия, модель поддерживает терапевтические подходы, направленные на модуляцию всего микробного сообщества с целью восстановления баланса, что потенциально может привести к более эффективному лечению.
Однако, эта модель может быть ограничена в учёте индивидуальных различий микробиома и иммунного ответа хозяина, что подчёркивает необходимость персонализированного подхода к лечению.
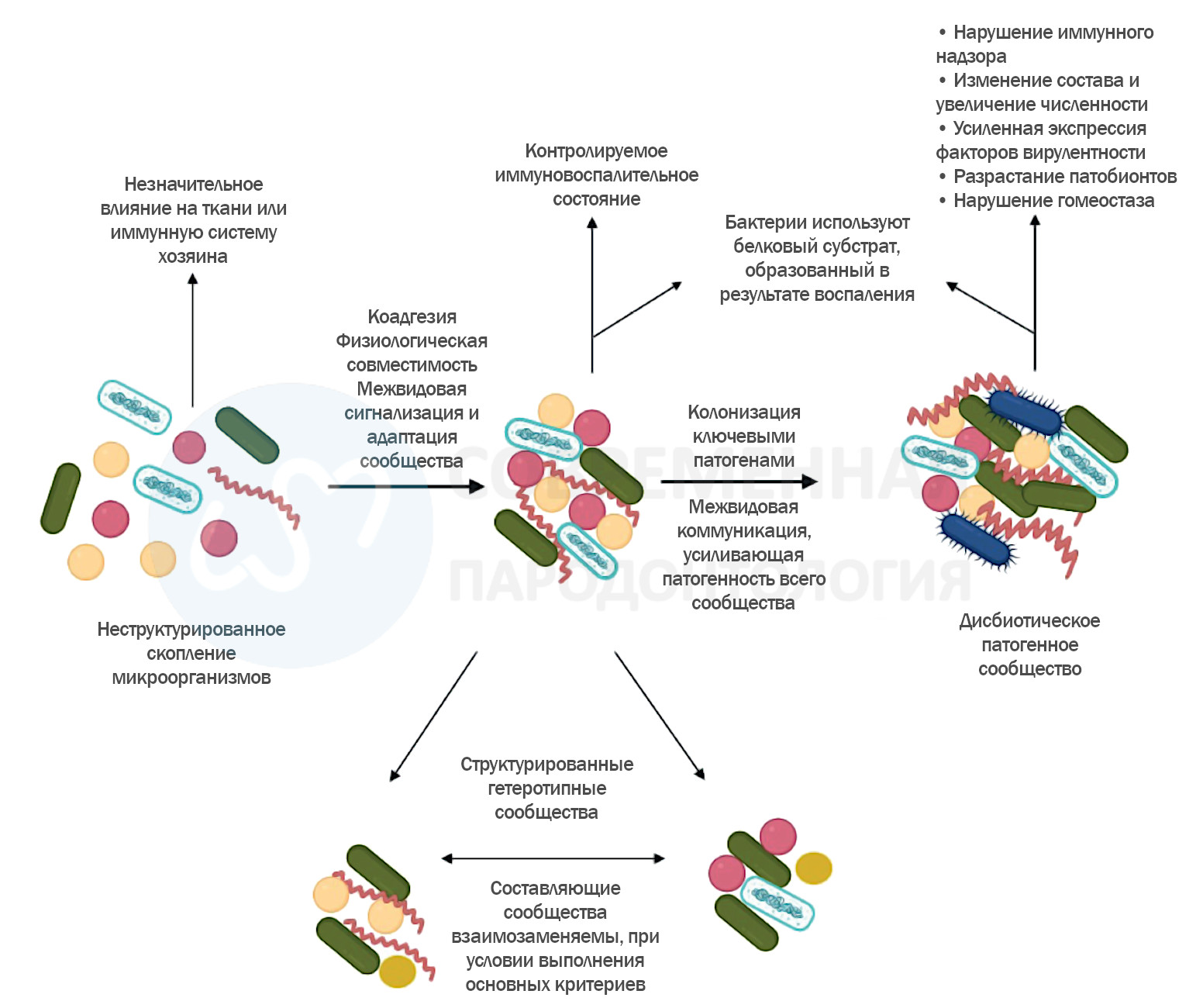
Рис. 1. Модель полимикробной синергии и дисбиоза рассматривает пародонтит как следствие действия не отдельных патогенов, а дисбиотической микробиоты, где метаболически совместимые микроорганизмы взаимодействуют и уклоняются от иммунного ответа. Процесс поддерживается ключевыми патогенами и сопровождается самоподдерживающимся циклом воспаления и потери кости
Современная модель
Современная модель патогенеза пародонтита, предложенная Мейле и Чапплом в 2015 году, ставит под сомнение традиционное представление о том, что пародонтит вызывается исключительно патогенной микрофлорой, провоцирующей воспаление. Вместо этого модель предполагает, что дисбиоз, аналогичный таковому при гингивите, начинается с воспалительного ответа со стороны хозяина.
Неспособность разрушить или удалить биоплёнку приводит к явному дисбиозу, который вызывает деструктивное, необратимое воспаление, характерное для пародонтита.
Эта модель рассматривает пародонтит как хроническое, саморазрушительное состояние, возникающее из-за неспособности разрешить чрезмерное воспаление. Подчёркивается взаимная связь между пародонтальной биоплёнкой и воспалительным иммунным ответом, при которой хозяин обеспечивает микроорганизмы питательными веществами, а микробы в биоплёнке стимулируют иммунный ответ хозяина.
Основное предположение модели состоит в том, что у предрасположенных индивидов переход от орального здоровья к гингивиту и в конечном итоге к пародонтиту связан с трансформацией биоплёнки: от состояния, поддерживающего здоровье, к состоянию начального дисбиоза и, в итоге, к выраженному дисбиозу.
Параллельно с этим воспалительный ответ хозяина изменяется от пропорционального и способствующего разрешению воспаления — к пропорциональному, но неразрешающему воспаление, и в итоге — к непропорциональному и неразрешающему.
Преимуществом модели является её комплексный подход, интегрирующий микробные, иммунные и экологические факторы для более тонкого понимания прогрессирования заболевания и различий в ответе на лечение.
Однако практическая реализация лечения по этой модели может быть затруднена из-за необходимости в современных диагностических инструментах и персонализированных стратегиях, учитывающих как микробные, так и иммунные особенности пациента.
Модель воспалительно-опосредованного полимикробного возникновения и усиления дисбиоза (IMPEDE)
Воспаление представляет собой защитную сосудистую и клеточную реакцию на раздражители и инфекции, способствующую выживанию и поддержанию тканевого гомеостаза при многих вредных воздействиях.
Контролируемая воспалительная реакция низкой интенсивности на биопленку может поддерживать гомеостаз тканей и предотвращать переход гингивита в пародонтит.
В соответствии с этим в 2020 году Ван Дайком и соавторами была предложена модель воспалительно-опосредованного полимикробного возникновения и усиления дисбиоза (IMPEDE), разработанная для поддержки внедрения Классификации пародонтита Всемирного семинара 2017 года.
Эта модель подчёркивает ключевую роль воспаления в запуске полимикробного дисбиоза и прогрессировании пародонтита.
Модель IMPEDE выделяет пять стадий на континууме от пародонтального здоровья до пародонтита, на каждой из которых заболевание может либо стабилизироваться, либо перейти на следующую стадию. Это:
- Стадия 0: пародонтальное здоровье;
- Стадия I: гингивит (воспаление);
- Стадия II: инициация/ранний пародонтит (возникает полимикробное разнообразие);
- Стадия III: воспалительно-опосредованный дисбиоз и оппортунистическая инфекция;
- Стадия IV: поздний пародонтит.
Ключевое положение модели IMPEDE заключается в том, что контролируемый, слабовыраженный воспалительный ответ на биопленку способен поддерживать гомеостаз тканей и предотвращать прогрессирование гингивита в пародонтит.
Соответственно, эффективный контроль и регуляция иммунного и воспалительного ответа хозяина играют решающую роль в предотвращении прогрессирования заболевания.
Напротив, дизрегулированный воспалительный ответ способствует прогрессированию болезни, поддерживая цикл воспалительно-опосредованного дисбиоза, который усиливает хроническое воспаление и прогрессирующее разрушение пародонтальных тканей.
Модель IMPEDE подчёркивает важность нацеливания на воспаление для разрыва этого порочного круга и снижения патогенеза пародонтита.
Сильные стороны модели включают акцент на роли воспаления как движущей силы дисбиоза. Однако её фокус на воспалении и дисбиозе может временами затмевать другие важные факторы, такие как генетическая предрасположенность или системные состояния, также играющие значительную роль в патогенезе пародонтита.
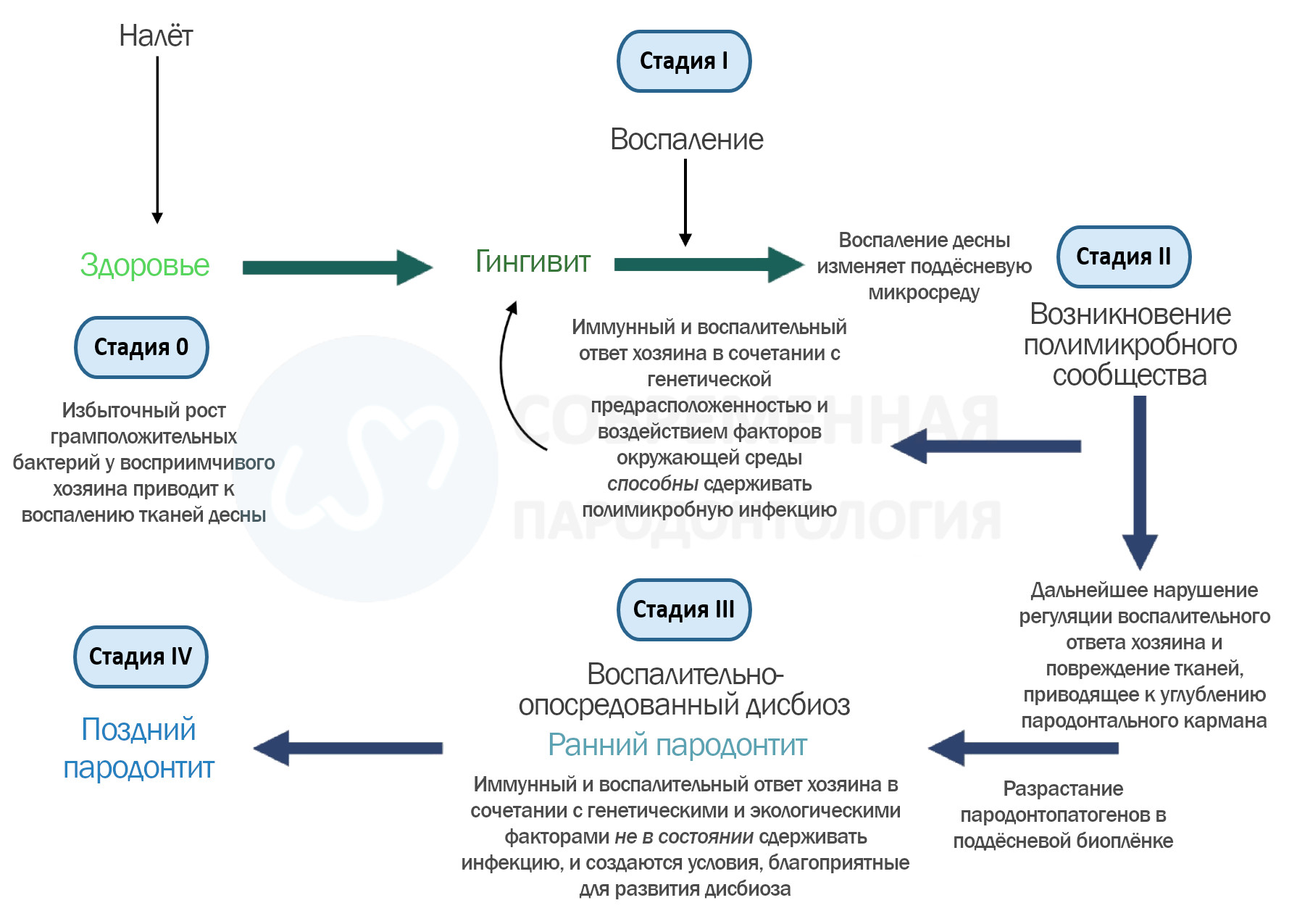
Рис. 2. Модель IMPEDE описывает пять стадий развития пародонтита: от здоровья до поздних форм заболевания. На каждом этапе воспаление может быть взято под контроль или усилено. Эффективное управление иммунным ответом препятствует прогрессированию, тогда как его дисрегуляция запускает порочный круг дисбиоза, хронического воспаления и разрушения тканей
Заключение
В целом, дентальная биопленка представляет собой сложное микробное сообщество, которое выступает в качестве основного этиологического фактора пародонтального заболевания, вызывая атипичный ответ организма.
Дисбиоз, характеризующийся нарушением как микробного состава, так и функции в составе биоплёнки, играет ключевую роль в прогрессировании заболевания. Модель ключевого патогена вносит современный взгляд, подчёркивая значительное влияние отдельных микробных видов на среду, несмотря на их низкую численность.
Недавно модель IMPEDE прояснила сложное взаимодействие между воспалением и дисбиозом, показав, как эти процессы совместно способствуют прогрессирующему характеру пародонтита. Эта модель приобретает всё большую популярность и, по-видимому, наиболее полно отражает патогенез пародонтита.
Поскольку микроорганизмы в составе биоплёнки обладают высокой устойчивостью к устранению только с помощью антимикробных средств, клиницисты должны осознавать важность регулярного профессионального механического удаления зубного налёта как неотъемлемой части лечения пародонтальных заболеваний.
Персистирующие бактерии, если их не удалять механически с несамоочищающихся поверхностей, таких как зубы, могут способствовать развитию болезни и дисбиоза.
Хотя некоторые бактерии находятся в симбиозе с хозяином, до сих пор неизвестно, какое их количество необходимо для перехода от состояния здоровья к заболеванию. Поэтому основной целью должно быть восстановление и поддержание микробиома в здоровом, сбалансированном состоянии.
Клиницисты должны консультировать пациентов по вопросам изменений образа жизни, таких как отказ от курения и улучшение контроля диабета, для поддержки здоровья полости рта и предотвращения дисбиоза.
Ограничение использования антибиотиков имеет решающее значение для предотвращения устойчивости бактерий и обеспечения эффективного лечения пародонтита.
По материалам Maryam Alshamsi, Emily Ming-Chieh Lu «Plaque Biofilm in Periodontitis: Past, Present and Future», 2025

Полностью согласна с тем, что необходимо достигнуть комплайенса — готовности пациента соблюдать врачебные рекомендации по тщательной гигиене полости рта и регулярному повторному обследованию на предмет качества гигиены, уровня гигиенического индекса, и, при необходимости, повторного тщательного удаления наддесневых и поддесневых зубных отложений, с последующим полированием и реминерализирующей терапией.