Медикаментозно-ассоциированный остеонекроз челюстей является относительно редким, но клинически значимым осложнением в стоматологии, которое создаёт существенные трудности в диагностике и лечении.
Медикаментозно-ассоциированный остеонекроз челюстей (MRONJ) чаще встречается у женщин и тесно связан с терапевтическим применением антирезорбтивных препаратов, таких как бисфосфонаты (BP) и деносумаб (DMB). Сообщаемая распространённость составляет менее 5% у пациентов, получающих антирезорбтивную терапию по поводу злокачественных новообразований, и ниже 0,05% у пациентов, лечащихся по поводу остеопороза или остеопении. Тем не менее в литературе описаны и более высокие показатели заболеваемости, до 17%, особенно при применении деносумаба.
С момента первых сообщений о MRONJ значительное количество исследований было посвящено изучению его этиологии, патофизиологии, профилактики и лечения. Несмотря на это, точные механизмы развития MRONJ остаются неясными. Эта неопределённость вызывает особую обеспокоенность, учитывая высокую распространённость заболеваний полости рта и частую необходимость удаления зубов — одного из наиболее распространённых триггеров развития MRONJ. Эти факторы дополнительно усложняют профилактику и лечение заболевания, что стимулировало применение консервативных нехирургических подходов, направленных на минимизацию обнажения кости. Однако такие меры не всегда возможны или рекомендованы, особенно в случаях обширной инфекции, поражающей пульпу или поддерживающие пародонтальные структуры. В подобных ситуациях они могут затруднять полноценную реабилитацию и не соответствовать ожиданиям пациента.
В этом контексте дентально-альвеолярные методы, такие как направленная регенерация тканей (GTR), которые предполагают хирургическое вмешательство и, следовательно, потенциально связаны с риском развития MRONJ, тем не менее могут обеспечивать клинические преимущества при аккуратном выполнении. К таким преимуществам относятся улучшение послеоперационного восстановления, сохранение зубов при выраженном пародонтальном поражении и поддержание объёма тканей в лунках после удаления зубов. Кроме того, достижения в области микрохирургии, поддерживаемые использованием увеличительной оптики, открывают возможность выполнения таких вмешательств менее инвазивно, минимизируя повреждение тканей и сохраняя структурную целостность.
Целью данного клинического наблюдения является описание потенциальной роли микрохирургических методик и регенеративных процедур в лечении пациентов с риском развития MRONJ.
Три репрезентативных клинических случая обширных костных дефектов, вызванных эндодонтическими и/ или пародонтальными заболеваниями и сопровождающихся высокой вероятностью потери объёма тканей, были отобраны среди пациентов с анамнезом приёма бисфосфонатов (BP) и/ или деносумаба (DMB). Пациенты наблюдались в частной клинике эндодонтии и пародонтологии (Paulínia, штат Сан-Паулу, Бразилия) в период с июня 2023 года по январь 2025 года.
Клиническая информация и изображения были получены из электронной медицинской карты и базы клинических фотографий. Оценка рисков обсуждалась между лечащими врачами-стоматологами, пациентами и их родственниками.
Все пациенты прошли микрохирургическое вмешательство с использованием стоматологического операционного микроскопа с учётом индивидуальных медицинских рекомендаций и с проведением антибиотикопрофилактики. Направленная регенерация тканей (GTR) включала
- применение EDTA 24% и производного эмалиевого матричного протеина для кондиционирования поверхности корня в области хирургического вмешательства;
- использование костного трансплантата;
- применение коллагеновой мембраны.
Послеоперационные назначения включали
- антимикробное полоскание (0,12% хлоргексидин два раза в день в течение одной недели);
- анальгетики (дипирон/метамизол 1000 мг три раза в день в течение 3 дней);
- противовоспалительные препараты:
- дексаметазон 4 мг два раза в день в течение 2 дней (случаи 1 и 3),
- либо нимесулид 100 мг два раза в день в течение 5 дней (случай 2).
Антибиотикотерапия (амоксициллин/клавуланат калия 875 мг/125 мг) назначалась на 7 дней, начиная за день до хирургического вмешательства.
Дополнительно проводилась фотобиомодуляционная терапия:
- ежедневно в течение первых 3 дней (808 и 660 нм, 100 мВт, 2 Дж на точку, 4 точки),
- затем еженедельно в течение 1 месяца (660 нм, 100 мВт, 2 Дж на точку, 4 точки).
Во всех случаях было получено информированное согласие пациентов на публикацию клинических данных.
Случай 1
72-летняя пациентка была направлена для обследования по поводу длительного анамнеза заболеваний пародонта, при этом единственной её жалобой было значительное накопление зубного камня. В её медицинском анамнезе отмечался остеопороз, по поводу которого проводилось лечение пероральными бисфосфонатами (алендронат 70 мг один раз в неделю в течение 7 лет), после чего был назначен деносумаб (60 мг каждые 6 месяцев на протяжении последних 1,5 лет). Кроме того, она принимала антикоагулянт (апиксабан) для профилактики тромбозов.
Клиническое и рентгенологическое обследование выявило генерализованное заболевание пародонта III стадии, рецессию десны, аномалию прикуса III класса и двусторонний перекрёстный прикус в боковых отделах. Пациентка не предъявляла симптомов, и потери зубов не наблюдалось. Зуб 17 имел отрицательный тест на витальность пульпы, подвижность III степени, гноетечение, травматическую окклюзию, выраженные поддесневые зубные отложения и полное обнажение небного корня. Конусно-лучевая компьютерная томография (CBCT) показала эндодонто-пародонтальное поражение, затрагивающее периапикальную область мезиально-щёчного (MB) и дистально-щёчного (DB) корней зуба и подтвердила полную костную деструкцию в области небного корня.
Существовал риск потери зуба, однако с учётом анамнеза антирезорбтивной терапии первоначально была выбрана консервативная тактика. Была проведена пародонтальная терапия всей полости рта (NSPT), после чего пациентка проходила регулярное поддерживающее пародонтологическое лечение (SPC) каждые 3 месяца. Было выполнено эндодонтическое лечение/перелечивание зубов 17.
Через 6 месяцев наблюдения у пациентки отмечался благоприятный пародонтологический ответ на лечение, при этом подвижность зуба 17 уменьшилась до I степени. Однако контроль биоплёнки на обнажённом небном корне оставался затруднённым, что привело к рекомендации выполнить резекцию небного корня зуба 17. С учётом сохранения периапикальной зоны и необходимости хирургического вмешательства также было предложено дополнительное хирургическое эндодонтическое вмешательство (апикоэктомия, ретроградная подготовка и пломбирование) на щёчных корнях для улучшения прогноза.
Под медицинским контролем было рекомендовано прекратить приём антикоагулянта за 24 часа до процедуры, и пациентка получила антибиотикопрофилактику. Во время операции была выявлена фенестрация верхнечелюстной пазухи с выделением серозного содержимого. Биоматериалы для направленной костной регенерации (GBR) были установлены без необходимости ушивания мембраны Шнайдера. Шинирование зуба было выполнено через 2 дня после операции. Несмотря на частичную потерю трансплантационного материала из-за трудностей его адаптации, при долгосрочном наблюдении было отмечено полное восстановление тканей, устранение как эндодонтической, так и пародонтальной инфекции, а также прекращение подвижности зуба.
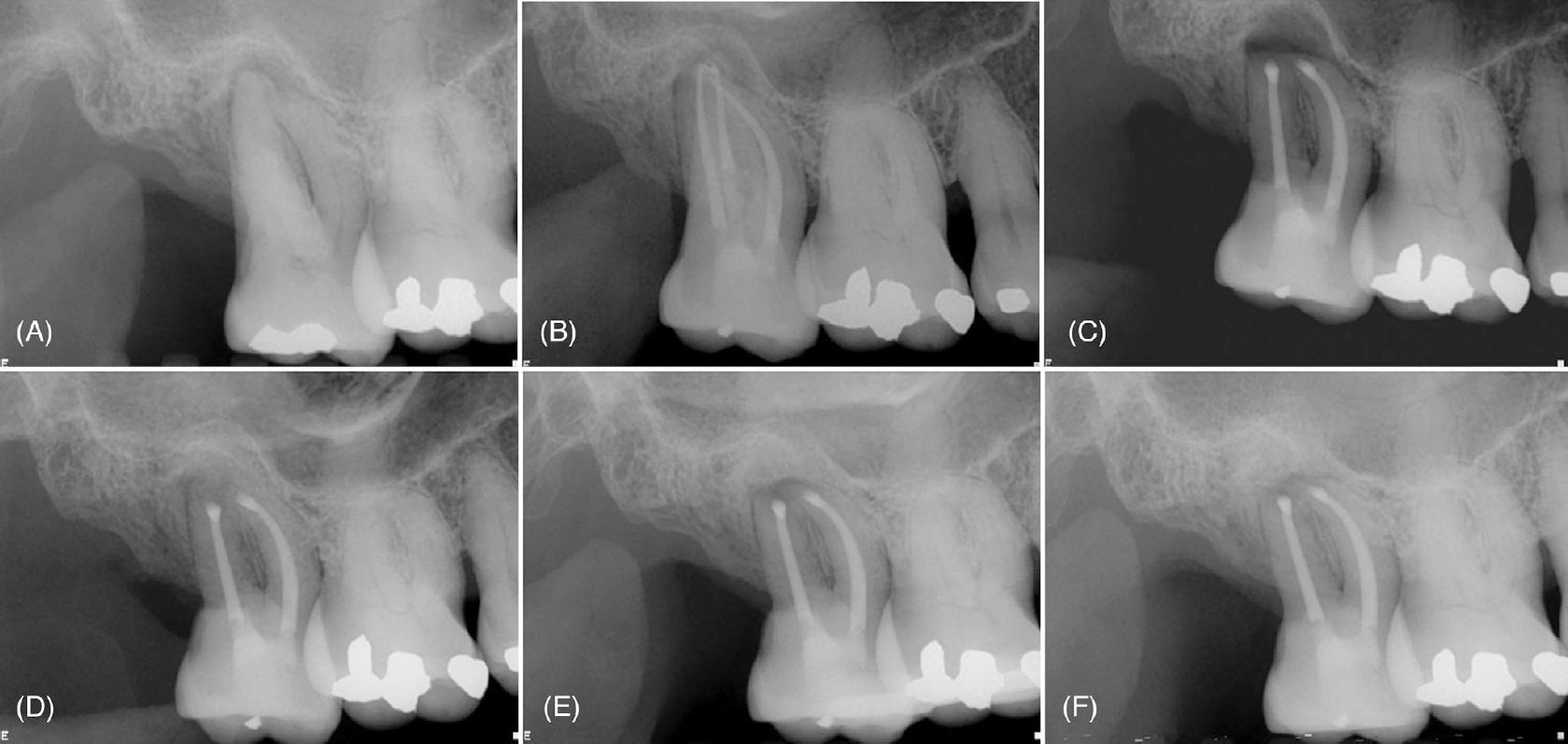
Фото 1. (A) Периапикальные рентгенограммы зуба 17 с рентгенопрозрачным очагом, окружающим корни, и (B) состояние после эндодонтического лечения корневых каналов. (C) Интраоперационная рентгенограмма после ретроградного препарирования и пломбирования щёчных каналов и полной резекции небного корня. (D) Непосредственная послеоперационная рентгенограмма после направленной костной регенерации. Рентгенограммы через 1 месяц (E) и 14 месяцев (F), демонстрирующие стабильное заживление и заполнение костного дефекта
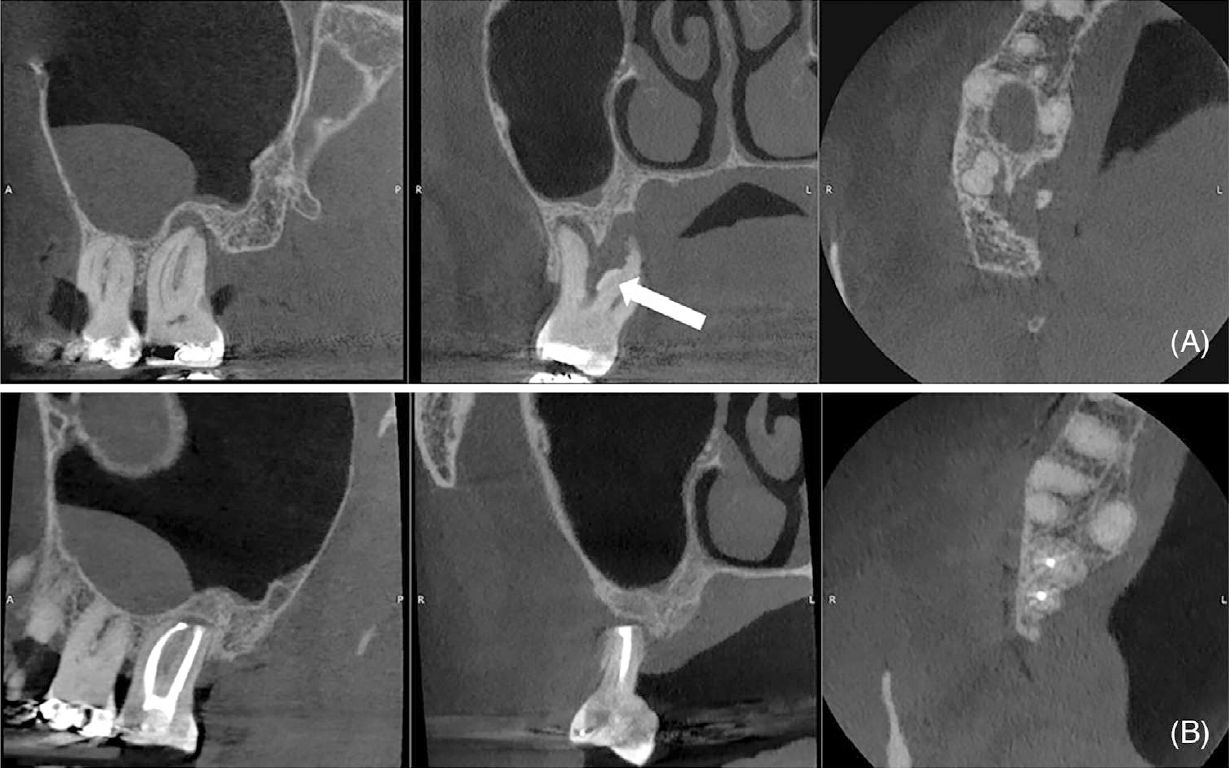
Фото 2. (A) Исходное КТ зуба 17 (сагиттальная, корональная и аксиальная проекции), демонстрирующее крупный участок сниженной плотности костной ткани, зубной камень (стрелка), кариес в области фуркации и сохранённую щёчную кортикальную пластинку. (B) КТ через 14 месяцев после операции (сагиттальная, корональная и аксиальная проекции), демонстрирующее образование кости на дистальной поверхности зуба 17 и ремоделирование апикальной и небной областей зуба 16. Линия, пониженной плотности, наблюдаемая в апикальной трети щёчных корней, соответствует репаративной ткани (коллагенизация)
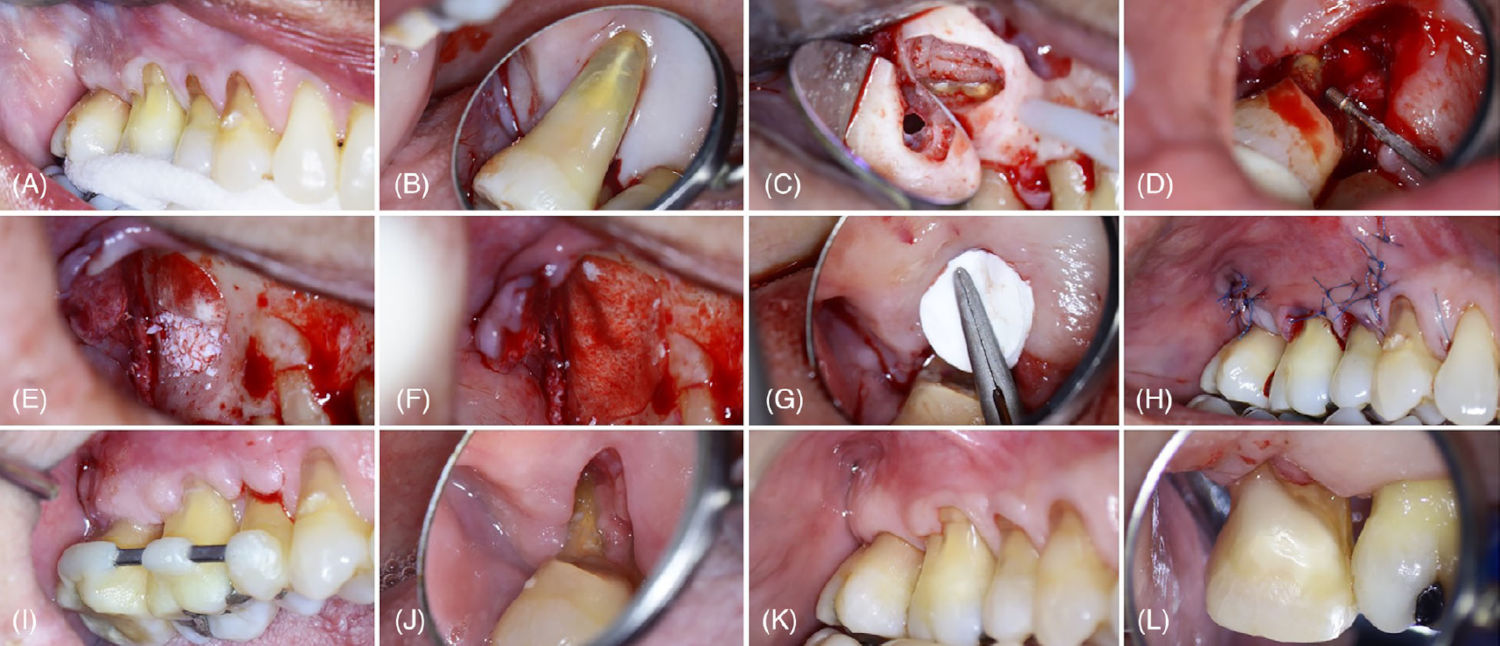
Фото 3. (A) Исходный вид со щёчной стороны. (B) Предоперационный небный вид после нехирургического обработки корней, демонстрирующий обнажённый небный корень. (C) Щёчные корни после апикоэктомии и ретроградного пломбирования, с перфорацией мембраны верхнечелюстной пазухи (вид через зеркало). (D) Резекция небного корня и сгаживание поверхности корня и области фуркации с использованием алмазных ультразвуковых насадок. (E) Размещение костного трансплантата. (F) Коллагеновая мембрана над трансплантатом. (G) Размещение коллагенового матрикса в области дефекта мягких тканей со стороны нёба. (H) Непосредственный послеоперационный вид с швами 6-0 из полипропилена. Вид со щёчной (I) и небной (J) сторон через 2 недели после операции после шинирования зубов и снятия швов. Вид со щёчной (K) и небной (L) сторон через 14 месяцев после операции, сразу после выполнения реставрации для облегчения гигиены
Случай 2
63-летняя пациентка была направлена из-за обширного поражения вокруг зуба 16, которое распространялось на соседние зубы и было обнаружено при плановом обследовании. Пациентка не предъявляла симптомов, поскольку эндодонтическое лечение зуба 16 было проведено более десяти лет назад.
В её медицинском анамнезе отмечались дегенеративный сколиоз, по поводу которого были выполнены множественные операции, артериальная гипертензия, гиперхолестеринемия, болезнь Паркинсона, остеопороз, гастрит и депрессия.
Пациентка принимала большое количество лекарственных препаратов (полипрагмазия), при этом для целей данного исследования особое внимание уделялось следующим препаратам: ацетилсалициловая кислота (100 мг — 1 таблетка в день), малат кальция + витамин D3 (250 мг + 2,5 мг — 1 таблетка в день), холекальциферол (5000 МЕ — 1 таблетка в день) и деносумаб (60 мг — каждые 6 месяцев на протяжении последних 2 лет).
В анамнезе у неё отмечались аллергические реакции на кетопрофен, клоназепам и гидрокортизон.
При клиническом, рентгенологическом и томографическом обследовании зуб 16 демонстрировал очень крупное комбинированное эндодонто-пародонтальное поражение, подвижность II степени, кровоточивость при зондировании и глубину зондирования вокруг зуба приблизительно 15 мм.
Тесты на витальность пульпы были положительными для зуба 17 и отрицательными для зубов 16 и 15. Несмотря на эти проблемы, в целом состояние полости рта пациентки было хорошим: все зубы были сохранены, а объём проведённого реставрационного лечения был минимальным. Начальное лечение включало профессиональную гигиену всей полости рта и проведение пародонтальной терапии (NSPT) в верхнем правом квадранте.
Было выполнено эндодонтическое лечение зуба 15, после чего проведена микрохирургическая операция, включавшая удаление зуба 16, а также апикоэктомию, ретроградное препарирование и пломбирование зуба 15. Дополнительно был выполнен кюретаж альвеолы, при этом признаков ороантрального сообщения выявлено не было.
После проведения направленной регенерации тканей (GTR) вестибулярный лоскут был разделён и перемещён для покрытия альвеолы. Временный протез был установлен только после полного закрытия раны. У пациентки наблюдалось как рентгенологическое, так и клиническое устранение инфекции.
Контрольное CBCT-исследование через 10 месяцев после операции подтвердило сохранение объёма костной ткани и полное устранение инфекции. В настоящее время пациентка не имеет симптомов и находится на этапе реабилитационного лечения.
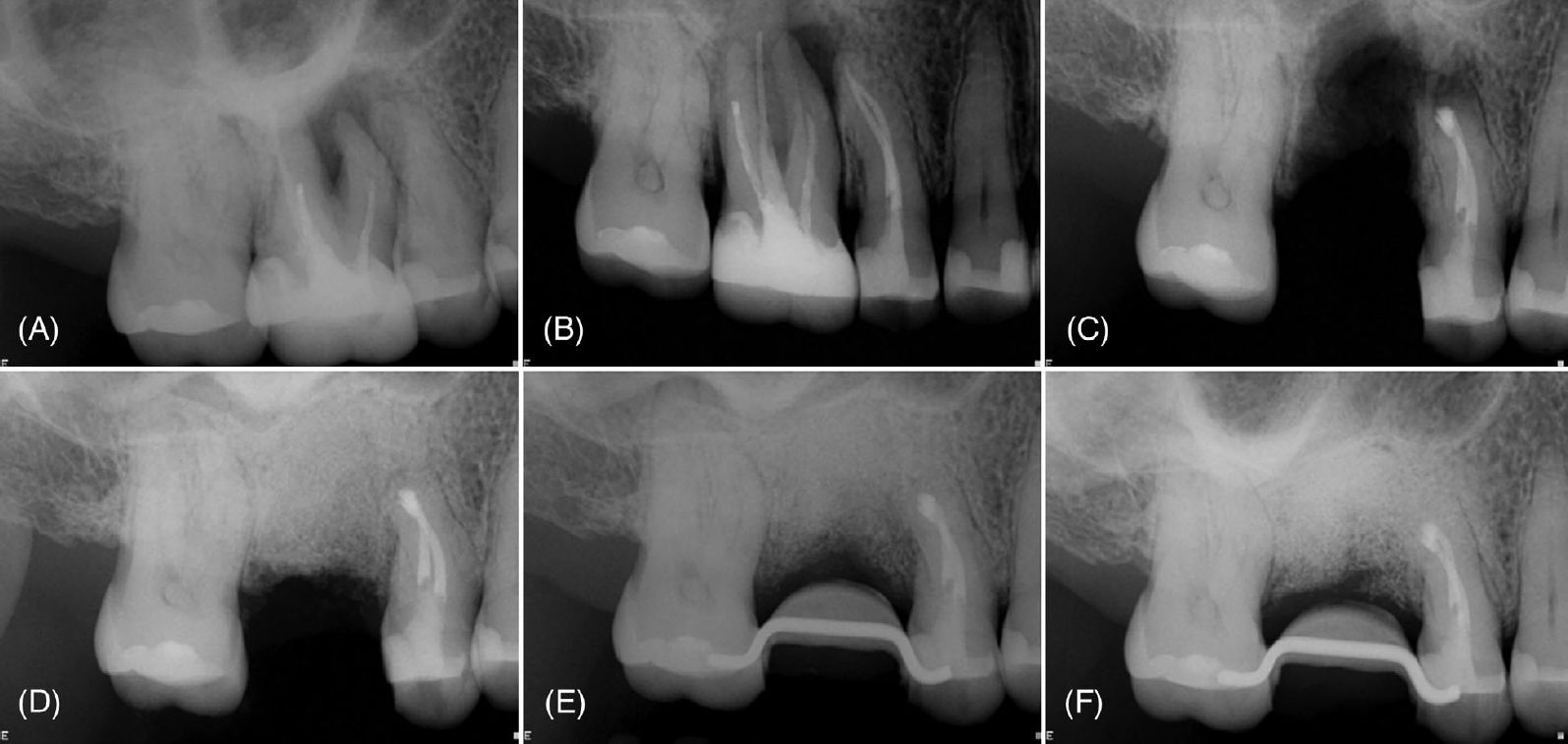
Фото 4. (A) Периапикальная рентгенограмма, демонстрирующая поражение, вовлекающее зубы 16 и 15. (B) Периапикальная рентгенограмма после эндодонтического лечения зуба 15. (C) Интраоперационная рентгенограмма после удаления зуба 16 и ретроградного пломбирования зуба 15. (D) Непосредственная послеоперационная рентгенограмма после направленной костной регенерации. (E) Рентгенограмма через 1 месяц наблюдения, выполненная после установки временной реставрации зуба 17. (F) Рентгенограмма через 8 месяцев наблюдения
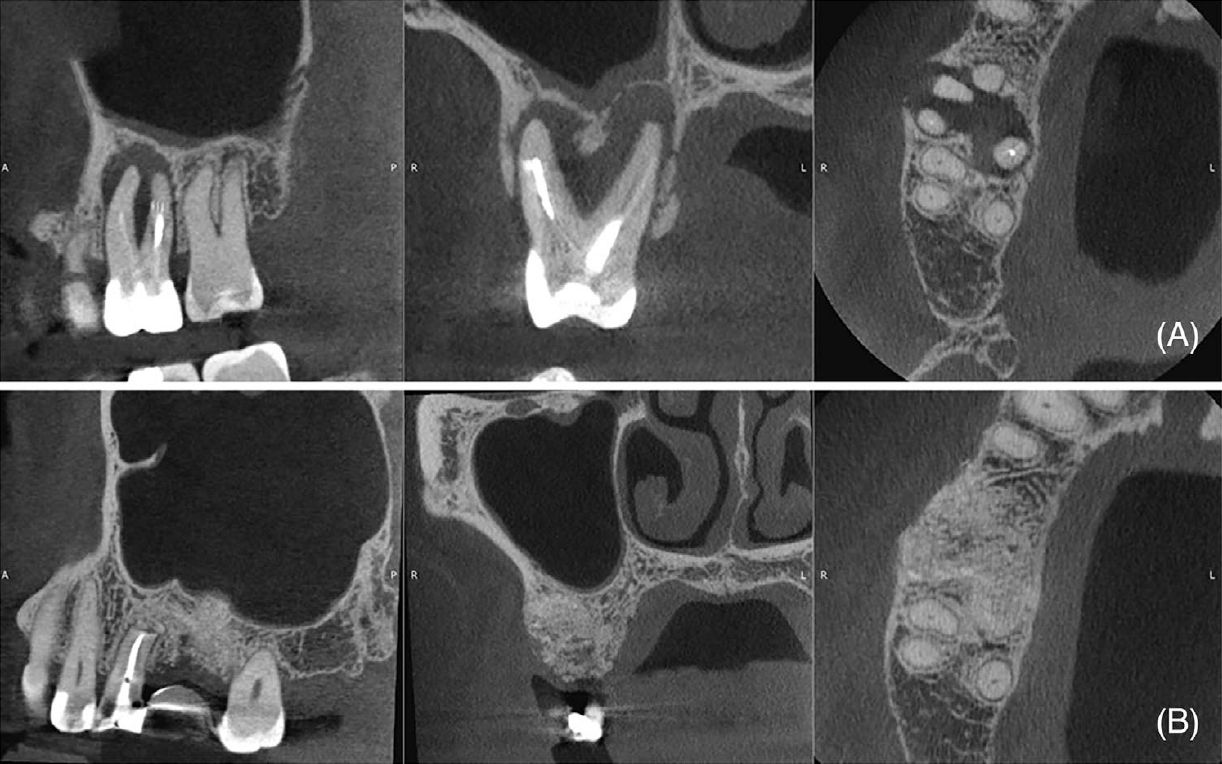
Фото 5. (A) Исходное КТ (сагиттальная, корональная и аксиальная проекции), демонстрирующее очаг пониженной плотности вокруг зубов 16 и 15, фенестрацию щёчной кортикальной пластинки и утолщение слизистой оболочки верхнечелюстной пазухи. (B) КТ через 10 месяцев после операции (сагиттальная, корональная и аксиальная проекции), демонстрирующее образование кости, апикальное ремоделирование зуба 15, сохранение объёма тканей и нормализацию состояния слизистой оболочки верхнечелюстной пазухи
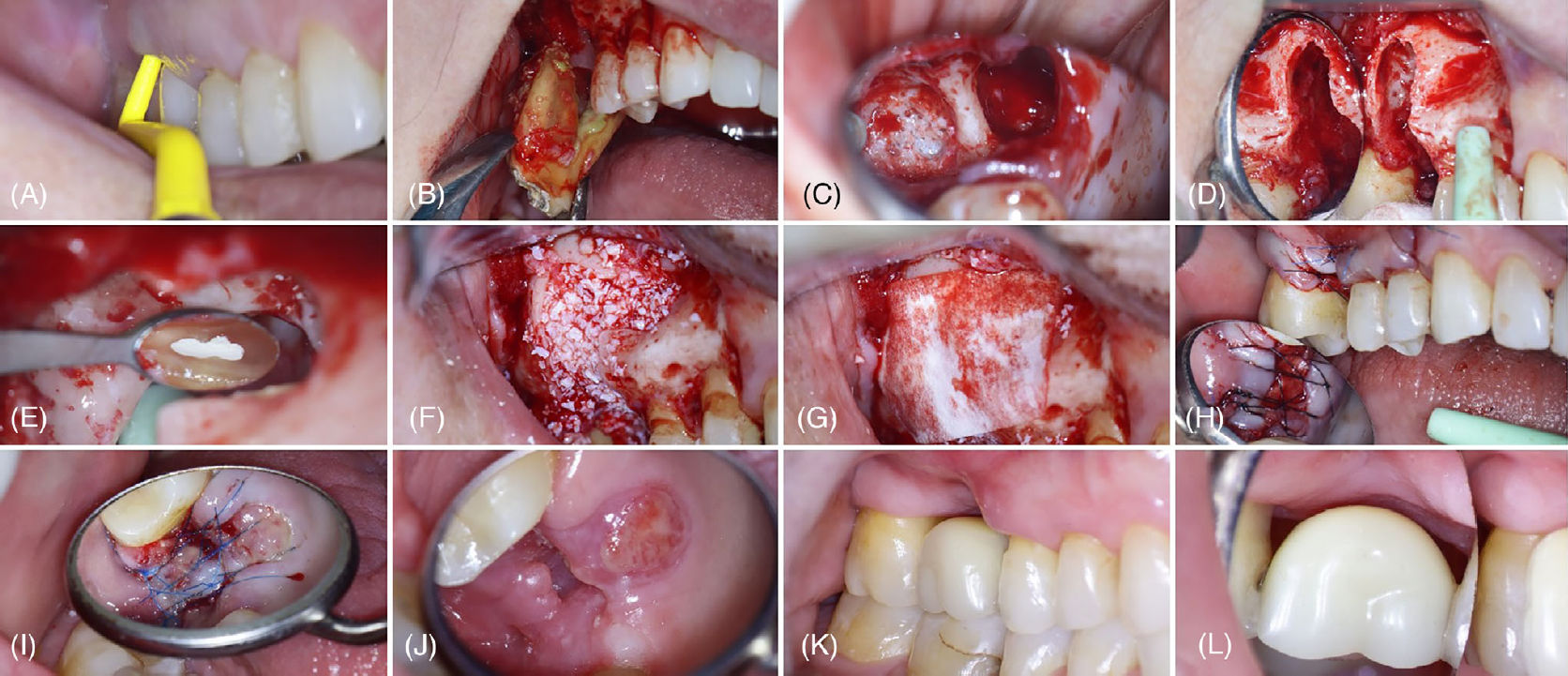
Фото 6. (A) Предоперационный вид со щёчной стороны зуба 16. (B) Удаление зуба 16, демонстрирующее гнойный экссудат и грануляционную ткань. (C) Альвеола после удаления и кюретажа с интактной кортикальной пластинкой верхнечелюстной пазухи. (D) Щёчный костный дефект. (E) Ретроградное пломбирование зуба 15 (вид через микрозеркало). (F) Размещение костного трансплантата. (G) Коллагеновая мембрана над костным трансплантатом. (H) Непосредственный послеоперационный вид со щёчной и окклюзионной сторон (вид через зеркало) с швами 6-0 из полипропилена и 6-0 из нейлона. (I) Окклюзионный вид через 1 неделю (I) и 2 недели (J) после операции. Вид со щёчной (K) и небной (L) сторон через 8 месяцев после операции. Временный протез был установлен через 1 месяц после операции
Случай 3
63-летняя пациентка была направлена в клинику для планового обследования, не предъявляя каких-либо конкретных жалоб. Клиническое и рентгенологическое обследование выявило необходимость замены нескольких неудовлетворительных реставраций и протезов.
Кроме того, в периапикальных областях зубов 18, 17 были выявлены очаги; все эти зубы ранее подвергались неадекватному эндодонтическому лечению.
В медицинском анамнезе пациентки был диагноз остеопороза, по поводу которого она получала лечение ибандронатом (150 мг один раз в месяц в течение 3 лет), затем ризендронатом (35 мг еженедельно в течение 2 лет), а в настоящее время получает деносумаб (60 мг каждые 6 месяцев).
Для оценки возможности проведения эндодонтического перелечивания зубов 18, 17 было выполнено исследование CBCT, и такая возможность была признана осуществимой. Первоначальные этапы лечения включали комплексную профессиональную гигиену полости рта, после чего были удалены неудовлетворительные протезные конструкции и реставрации. Стандартное эндодонтическое перелечивание было успешно выполнено для зуба 18, поскольку структура его корня оставалась интактной.
Однако, несмотря на попытку консервативного лечения, после снятия неудовлетворительной коронки у зуба 17 была выявлена обширная вертикальная трещина корня, что сделало перелечивание невозможным. Было проведено микрохирургическое вмешательство, включавшее удаление зуба 17, апикальный кюретаж зуба 18 и сглаживание поверхности корня для зубов 18 и 15.
Во время люксации зуба 17 произошёл перелом альвеолярной стенки, однако повреждения мембраны верхнечелюстной пазухи не было, что подтвердило возможность выполнения направленной костной регенерации (GBR) и синус-лифтинга через латеральную стенку альвеолы. Хотя процесс заживления был несколько более длительным, пациентка не испытывала болевых ощущений.
Через 3 месяца было отмечено полное восстановление тканей с сохранением объёма как мягких, так и твёрдых тканей, что позволило установить временный протез. Лечение продемонстрировало полное устранение инфекции и значительное заживление тканей.
В настоящее время пациентка находится под наблюдением, и в будущем планируется проведение аналогичных процедур на противоположной стороне зубной дуги.
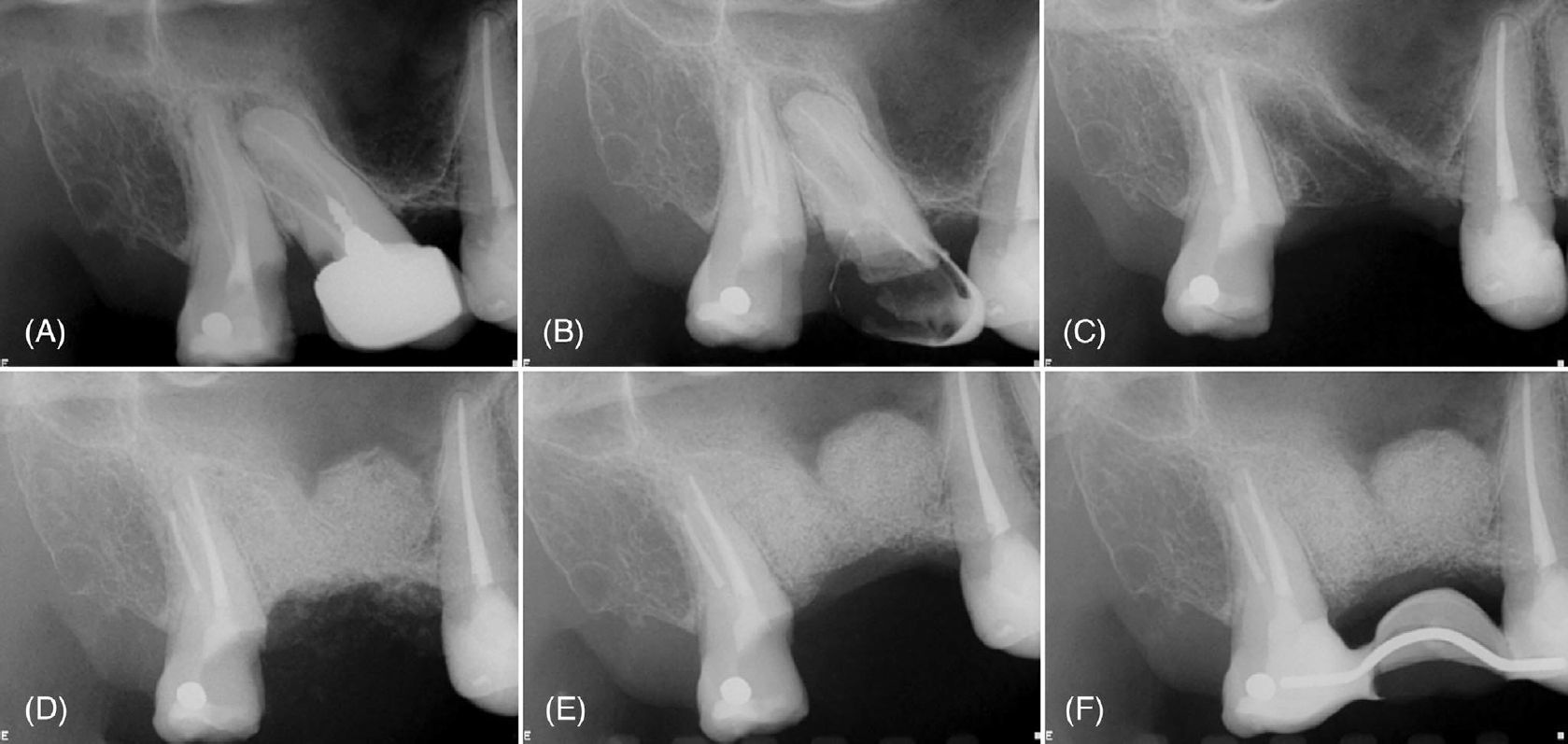
Фото 7. (A) Периапикальная рентгенограмма с рентгенопрозрачным очагом в периапикальной области зубов 18 и 17, кариес, дефектные реставрации и неудовлетворительное эндодонтическое лечение. (B) Периапикальная рентгенограмма после эндодонтического перелечивания зуба 18. (C) Интраоперационная рентгенограмма после удаления зуба 17, кюретажа альвеолы и апикопластики зуба 18. (D) Непосредственная послеоперационная рентгенограмма после костной регенерации и синус-лифтинга. Рентгенограммы через 1 месяц (E) и 3 месяца (F) наблюдения
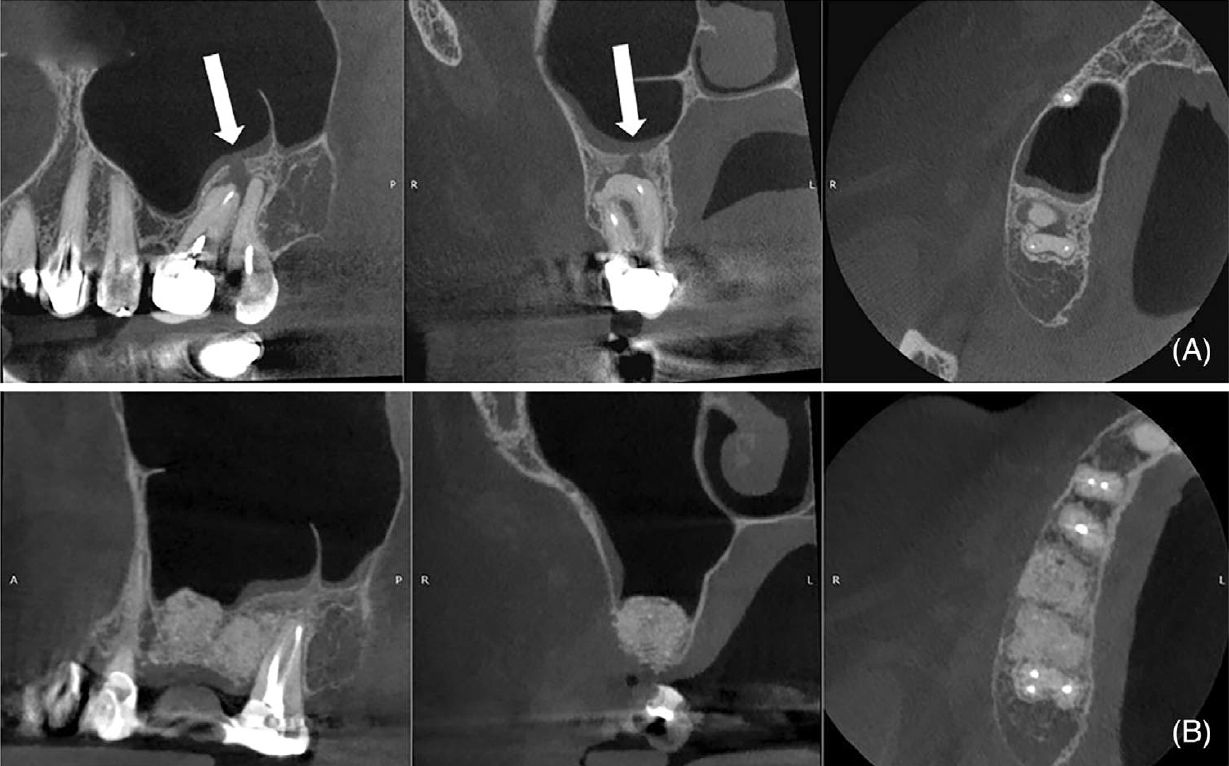
Фото 8. (A) Исходное КТ (сагиттальная, корональная и аксиальная проекции), демонстрирующее очаг пониженной плотности в области зубов 18 и 17, утолщение слизистой оболочки верхнечелюстной пазухи, кортикальную фенестрацию и ороантральное сообщение (стрелки). (B) КТ через 6 месяцев после операции (сагиттальная, корональная и аксиальная проекции), демонстрирующее образование кости, нормализацию состояния слизистой оболочки пазухи, восстановление кортикальной пластинки и закрытие ороантрального сообщения
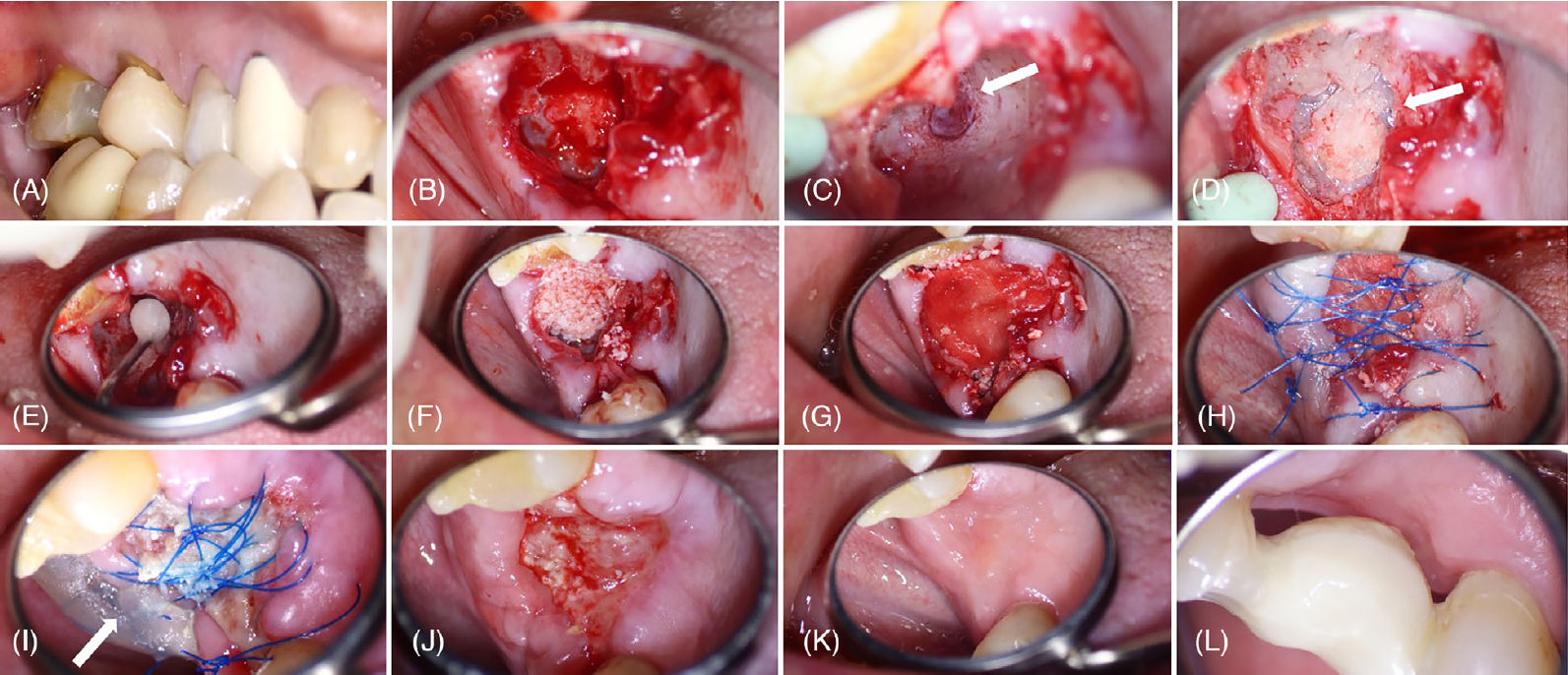
Фото 9. (A) Предоперационный вид со щёчной стороны зуба 17. Альвеола после удаления зуба 17 до (B) и после (C) удаления грануляционной ткани, демонстрирующая перфорированную кортикальную пластинку пазухи и интактную мембрану пазухи (стрелка). (D) Окклюзионный вид перелома кортикальной пластинки, прилежащей к мембране пазухи (стрелка). (E) Нанесение производного эмалиевого матричного протеина на поверхность корня зуба 18 (вид через зеркальце). (F) Размещение костного трансплантата. (G) Коллагеновая мембрана над костным трансплантатом. (H) Непосредственный послеоперационный окклюзионный вид (через зеркало) с швами 6-0 из полипропилена. (I) Окклюзионный вид через 1 неделю после операции, демонстрирующий размещение гингивального барьера на швах (стрелка) из-за травмы щёчной слизистой оболочки. Окклюзионный вид через 2 недели (J) и 45 дней (K) после операции. (L) Небный вид через 75 дней после операции, после установки временного протеза
Обсуждение
Успешное разрешение представленных клинических случаев подчеркивает эффективность хорошо структурированного подхода к лечению пациентов с риском развития MRONJ. Как сообщают Ruggiero и соавт. (2022), предшествующие воспалительные состояния, такие как заболевания пародонта или периапикальная патология, признаны факторами риска развития MRONJ. Учитывая ожидания пациентов по устранению инфекции при максимальном сохранении зубов, первоначально были разработаны индивидуализированные консервативные планы лечения, включавшие эндодонтическое лечение и нехирургическую пародонтальную терапию (NSPT), с последующим поддерживающим пародонтологическим лечением (SPC). Однако из-за персистирующей инфекции или осложнений хирургическое вмешательство в конечном итоге стало необходимым. На этом этапе опасения относительно потери объёма тканей, наряду с ожиданиями пациентов относительно функционального и эстетического улучшения, требовали тщательного баланса между риском развития MRONJ и преимуществами регенеративных хирургических методик.
Было отмечено несколько ключевых особенностей: все пациенты были женщинами старше 60 лет, с анамнезом терапии бисфосфонатами (BP) и деносумабом (DMB) по поводу остеопороза — состояния, связанного с более низким риском MRONJ по сравнению со злокачественными заболеваниями. Поражения локализовались в верхней челюсти, где осложнения MRONJ встречаются реже, чем в нижней челюсти.
Для дополнительного снижения риска MRONJ всем пациентам, у которых приближался очередной полугодовой приём деносумаба, было рекомендовано под медицинским контролем отложить его на 3 месяца, что превышает минимальную отсрочку в 1 месяц, предложенную Campisi и соавт. Для оптимизации хирургических результатов был реализован комплексный предоперационный протокол, включавший тщательную гигиену полости рта, контроль зубного налёта и антимикробную терапию. Кроме того, для ускорения заживления и уменьшения послеоперационного дискомфорта также применялась фотобиомодуляция.
Хотя точная патофизиология MRONJ остаётся неясной, было предложено несколько механизмов, включая прямую токсичность бисфосфонатов для слизистой оболочки полости рта, изменение иммунных реакций, ингибирование ангиогенеза и нарушение заживления ран.
Woo и соавт. также связывают особую уязвимость челюстей с более высокой скоростью костного ремоделирования и тонким слизистым барьером, который в норме предотвращает микробную инвазию.
Эти факторы создают биологически неблагоприятную среду для восстановления и регенерации тканей, что делает хирургические и регенеративные методы лечения в целом противопоказанными у пациентов с риском MRONJ. Однако данные литературы показывают, что при уже сформировавшемся MRONJ хирургическое вмешательство приводит к лучшим результатам.
Описанные подходы включают локальную обработку, остеопластику, сегментарную остеотомию и реконструкцию свободными васкуляризованными тканевыми лоскутами, поскольку нехирургические методы лечения часто не обеспечивают полного заживления поражения. В этом контексте минимально инвазивные хирургические техники и регенеративные процедуры рассматриваются как стратегии для лечения костных дефектов пародонтального и эндодонтического происхождения, делая такие вмешательства более эффективными и менее травматичными.
Улучшая визуализацию, использование увеличительных инструментов, таких как хирургические лупы и стоматологические операционные микроскопы, позволяет выполнять более точные манипуляции с тканями, ускоряет восстановление и снижает вероятность осложнений. Такие подходы могут иметь особые преимущества у пациентов с риском MRONJ, поскольку соответствуют принципам снижения хирургической травмы и создания благоприятных условий для заживления.
Кроме того, обнадёживающие результаты были получены у пациентов с риском MRONJ при проведении таких процедур, как вертикальная аугментация альвеолярного гребня с использованием костных трансплантатов и титановой сетки, применение аллопластических трансплантатов, расщепление гребня верхней челюсти, установка имплантатов, использование мезенхимальных клеток в сочетании с гетерологичной костью, а также применение фибрина, обогащённого тромбоцитами (PRF), для заживления ран и регенерации тканей. Одно экспериментальное исследование на животных дополнительно показало, что трансплантаты улучшают ремоделирование кости даже при наличии антирезорбтивной терапии.
Помимо хирургических аспектов, ведение пациентов с риском MRONJ также включает работу с их представлениями об антирезорбтивной терапии.
В некоторых случаях чрезмерные опасения по поводу развития MRONJ могут приводить к тому, что пациенты прекращают или отказываются от лечения, что потенциально снижает терапевтическую пользу этих препаратов. Эффективная медицинская помощь должна быть направлена не только на предотвращение осложнений MRONJ, но и на учёт долгосрочных потребностей пациентов в реабилитации, а также на включение их предпочтений в процесс принятия лечебных решений.
Пациентам данной категории часто рекомендуют удаление зуба как окончательное решение, что может представлять собой чрезмерное лечение, особенно когда возможны консервативные или минимально инвазивные альтернативы. Если хирургическое вмешательство уже необходимо, следует стремиться минимизировать его инвазивность, одновременно интегрируя методы, поддерживающие оптимальное состояние полости рта и общее качество жизни пациента.
По материалам Pedro Franco Ferreira et al., “Management of severe bone loss in patients at risk of medication-related osteonecrosis of the jaw with microsurgery and guided bone regeneration: A case study», 2026
