Мукозит в области установленных имплантов обычно вызван накоплением биопленки, которое нарушает гомеостаз в системе «организм хозяина-микробы» на границе импланта и слизистой оболочки, что приводит к воспалительному поражению.
Резюме
Цели
Этот описательный обзор был подготовлен для Всемирной конференции 2017 года Американской академии пародонтологии и Европейской федерации пародонтологов для решения ключевых вопросов, связанных с таким клиническим состоянием как мукозит в области имплантов, включающих: 1) определение мукозита, 2) переход из состояния здоровья тканей, окружающих имплант, в состояние мукозита (воспаления), вызванного биопленкой 3) обратимость мукозита 4) длительность течения мукозита в области имплантов 5) сходство и различия между мукозитом в области имплантов и гингивитом в области естественных зубов 6) показатели и факторы риска в развитии мукозита.
Методы
Поиск литературы в базах MEDLINE (PubMed) и The Cochrane Library, опубликованной до 31 июля 2016 года, был проведена с использованием стратегии поиска, включающей следующие ключевые слова и фразы: «периимплантит» (все упоминания), «мукозит или периимплантит» и «мукозит».
Были изучены все перспективные, ретроспективные и обзорные работы, в которых основное внимание уделялось факторам риска / показателям для мукозита, а также экспериментальные исследования мукозита у животных и с участием людей.
Результаты
Мукозит в области импланта — это воспалительное поражение мягких тканей, окружающих установленные внурикостно импланты, при отсутствии потери опорной кости или прогрессирующей потери маргинальной кости.
Была продемонстрирована причинно-следственная связь между экспериментальными ростом бактериальной биопленки вокруг титановых дентальных имплантатов и развитием воспалительного ответа. Экспериментальный периимплантный мукозит характеризуется наличием воспалительного клеточного инфильтрата в соединительной ткани латерально относительно барьерного эпителия. При мукозите, протекающем длительный период времени инфильтрат воспалительных клеток больше по размеру, чем в раннем (3-недельнем) экспериментальном мукозите в области имплантов. Мукозит, вызванный биопленкой, является обратимым на уровне биомаркеров организма хозяина после восстановления контроля над биопленкой. Клинические признаки воспаления могут проявиться через более чем 3 недельный срок. Факторы, определенные как факторы риска для мукозита, включают в себя накопление биопленки, курение и радиация. Дополнительные доказательства требуются для так называемых потенциальных факторов риска, включая диабет, недостаток ороговевшей слизистой оболочки и наличие избыточного цемента (материала).
Выводы
Мукозит в области установленных имплантов вызван накоплением биопленки, которое нарушает гомеостаз в системе «организм хозяина-микробы» на границе импланта и слизистой оболочки, что приводит к воспалительному поражению. Мукозит является обратимым состоянием на уровне биомаркеров хозяина. Таким образом, клинически важным является то, что оптимальное удаление биопленки является важной предпосылкой для профилактики и лечения мукозита. Понимание такого состояния как мукозит очень важно, потому что это состояние считается предшественником периимплантита.
Ключевые слова
Заболевания в области имплантов, мукозит, периимплантит, фактор риска, индикатор риска
Заболевания, в том числе периимплантационный мукозит и периимплантит, были впервые описаны на Первом Европейском семинаре по вопросам пародонтологии в Иттингене в 1993 году. После этого, было проведено множество семинаров, посвященных определению, распространенности и лечению этих заболеваний. Периимплантационный мукозит считается предшественником периимплантита. Цель этого обзора заключается в том, чтобы рассмотреть следующие ключевые вопросы: 1) определение мукозита, 2) переход из состояний здоровья в мукозит, индуцированный биопленкой, 3) обратимость мукозита, 4) длительно протекающее состояние мукозита, 5) сходства и различия между мукозитом в области имплантов и гингивитом у зубов, 6) факторы риска в отношении мукозита.
Материалы и методы
Поиск литературы в базах MEDLINE (PubMed) и The Cochrane Library, опубликованной до 31 июля 2016 года, был проведена с использованием стратегии поиска, включающей следующие ключевые слова и фразы: «периимплантит» (все упоминания), «мукозит или периимплантит» и «мукозит». Было обнаружено 224 статьи по заданным критериям.
Были изучены все перспективные, ретроспективные и обзорные работы, в которых основное внимание уделялось факторам риска / показателям для мукозита, а также экспериментальные исследования мукозита у животных и с участием людей.
После соответствующего обсуждения нынешние авторы согласились с ранее проведенными исследованиями и включили их в этот описательный обзор, основанный на выше изложенных вопросах, посвященных теме мукозита.
Мукозит: определение
Периимплантационный мукозит был определен на предыдущих семинарах как воспалительное поражение слизистой оболочки, окружающей эндоосальный имплант без потери поддерживающей костной ткани. Важным критерием определения мукозита являются воспаление в слизистой оболочке, окружающей имплант и отсутствии прогрессирующей потери маргинальной костной ткани. Клиническим признаком воспаления является, прежде всего, кровотечение при зондирование, в то время как дополнительными признаками могут быть покраснение, отек и нагноение.
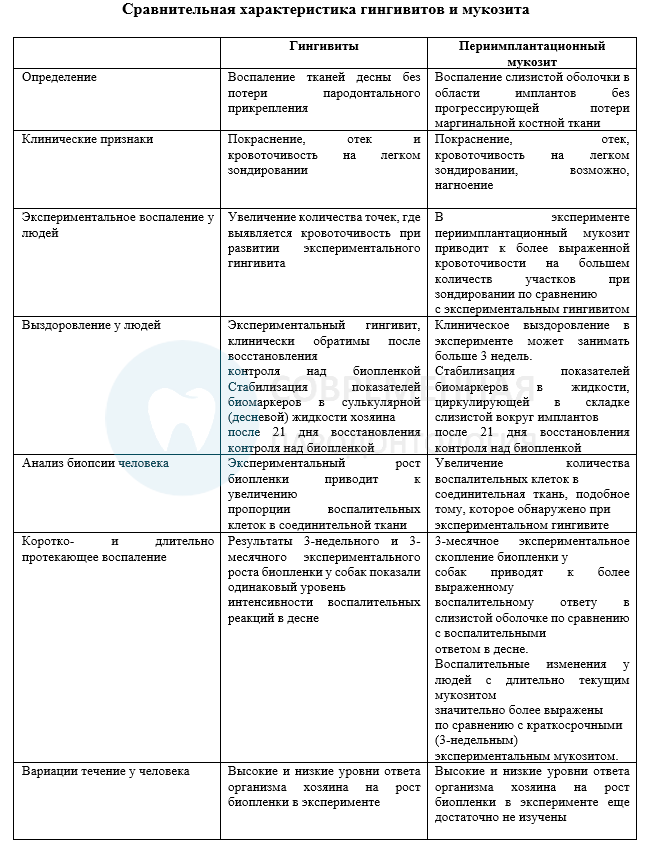
Переход от здоровой слизистой оболочки в области имплантов к периимплантационному мукозиту
Здоровая слизистая оболочка в области импланта характеризуется наличием эпителия полости рта, распространяющимся до некератинизированного барьерного эпителий с базальной пластинкой и гемидомосомами, обращенными к имплантату или поверхности абатмента. В соединительной ткани, прилегающей к барьерному эпителию, присутствуют клетки воспалительного инфильтрата, представляющие защиту хозяина от бактериального поражения. В состоянии здоровья слизистой оболочки, барьерный эпителий и рассеянные клетки воспаления образуют мягкотканную изоляцию, разделяющую периимплантное прикрепление и полость рта.
Мукозит развивается из здоровой слизистой оболочки вокруг имплантата после накопления бактериальных биопленок вокруг остеоинтегрированных зубные имплантов. Причинно-следственная связь между экспериментальным накоплением бактериальных биопленок вокруг титана зубных имплантов и развитием воспалительного ответа (то есть экспериментальный периимплантный мукозит) была продемонстрирована с участием человека. В раннем исследовании Pontoriero et al., наблюдались пациенты с частичным отсутствием зубов после пародонтальной терапии, которым были установлены импланты. После 6 месяцев контролируемой гигиены полости рта, слизистая оболочка в области имплантов характеризовалась отсутствием очевидных признаков клинического воспаления. После этого периода пациентов просили отменить гигиену полости рта в течение 3 недель. В конце этого периода был восстановлен оптимальный контроль биопленки. На всех обследованиях были отмечены следующие клинические параметры вокруг имплантатов: индекс бляшки (PI), гингивальный индекс (GI), кровоточивость при зондировании (SBI), глубина зондирования (PD) и маргинальная рецессия (REC). Проведен трехнедельный период отмены гигиены полости рта и наблюдалось развитие видимых признаков воспаления слизистой оболочки, таких как отек, покраснение и кровотечение. Эта причинно-следственная связь между накоплением бактериальных биопленок и развитие мукозита согласуется с результатами, полученными в модели экспериментального гингивита Löe et al.
В другом исследование Zitzmann et al. было изучено 12 пациентов с частичным отсутствием зубов и признаками воспаления. Воспалительный ответ на экспериментальный бактериальную агрессию характеризовался изменением пропорции Т- и В-клеток в тканях, окружающих импланты. Биопсия, полученная из тканей окружающие импланты в клинически здоровой ситуации и после 21 день экспериментального накопления биопленки, показала, что соединительная ткань, окружающая имплантаты, показала увеличенный объем Т- и В-лимфоцитов вследствие отмены гигиены полости рта. Было также отмечено, что размер воспалительного клеточного инфильтрата и количества нескольких популяций иммунных клеток отличался незначительно при сравнении данных биопсии десны вокруг естественных зубов и биопсии из слизистой оболочки в области имплантов.
Результаты сравнительного исследования на людях Salvi et al. показали, что 3 недели экспериментального накопления биопленки привели в большей доле кровоточивости в слизистой оболочке, вокруг имплантов по сравнению с таковой в десне. В этом исследовании индекс гигиены в области зубов был значительно увеличен по сравнению с ситуацией вокруг имплантов после 3 недель отмены гигиены полости рта. Однако увеличение GI на участках, где были естественные зубы, было значительно ниже по сравнению с участками в области имплантатов, что в свою очередь указывает на то, что сопоставимая бактериальная агрессия дает более сильный воспалительный ответ на участках, где имеются импланты.
Недавнее исследование, проведенное Meyer et al., поставило задачей сравнить клинические и биологические ответы во время экспериментального гингивита и периимплатного мукозита у людей в возрасте ≥70 лет. Хотя наблюдалось меньшее накопление биопленки на участках, где установлены имплантаты, слизистая оболочка в этой же области давала более высокую показатель кровоточивости по сравнению с таковой, наблюдаемой в области десны естественных зубов. Таким образом, были подтверждены результаты Salvi et al., полученные в группе более молодых пациентов.
Мукозит, вызванный биопленкой, обратимое заболевание?
Хотя причинно-следственная связь между экспериментальным накоплением биопленки и развитием периимплантного мукозита была доказана в двух упомянутых ранее исследованиях, описание достоверных причинно-следственных связей по этому вопросу укрепили бы доказательства об обратимости воспалительного процесса до пред-экспериментального уровня здоровья слизистой оболочки. В исследовании Salvi et al. GI в области имплантов был значительно меньше по сравнению с таковым в области зубов после 3 недель восстановленной практики гигиены полости рта. Кроме того, уровни GI (на до экспериментальном уровне) не достигались на участках, где имелись импланты через 21 день после восстановления контроля биопленки. Это указывало на то, что разрешение экспериментального мукозита у людей может занимает более 3 недель. В отличие от исследования Salvi et al все клинические параметры, оцененные у пожилых пациентов (т. е. ≥70 лет) вернулись на пред- экспериментальные уровни через 3 недели восстановления контроля биопленки, тем самым доказывая обратимость экспериментально индуцированного мукозита.
Было достигнуто разрешение (выздоровление) экспериментального мукозита в обоих исследованиях на уровне биомаркеров хозяина. Доказано уменьшение до пред- экспериментальных значений уровня биомаркеров в десневой жидкости. Эти результаты подтвердили выводы другого исследования, в котором оценивались уровни интерлейкина (IL) -1β, фактора некроза опухолей- альфа (TNF-α) и трансформирующего фактор роста-бета2 (TGF-β2) в десневой жидкости у 25 испытуемых до и после 3-недельного периода отмены гигиены полости рта и через 69 дней после ее восстановления. Хотя уровни TNF-α и TGF-β2 не изменялись значительно в течение экспериментального периода, IL-1β значительно увеличивался после 3 недель отмены гигиены полости рта и вернулся до пред-экспериментальных значений через 69 дней. Хотя период восстановления гигиены полости рта был короче на 3 недели в исследованиях Salvi et al. и Meyer et al., уровень IL-1β в десневой жидкости вернулся к предварительным значениям, подтвердив тем самым результаты полученные Schierano et al.
Модель экспериментального мукозита в сравнении с длительно текущим периимплантационным мукозитом
Экспериментальные исследования на животных и с участием человека показали, что накопление биопленки de novo приводит к воспалительному поражению слизистой оболочки вокруг установленных имплантов с миграцией лейкоцитов через барьерный эпителий и формирование воспалительного инфильтрата с увеличением доли Т- и В-клеток в соединительной ткани, прилегающей к барьерному эпителию.
Исследования на животных
В экспериментальных моделях периимплантационных мукозитов оцениливались реакция слизистой оболочки в области импланта как на ранней (3 недели), так и на поздней фазе (90 дней) при ненарушенной структуре биопленки. В этих исследованиях на собаках были проведены сравнения между ответами со стороны десны, окружающей естественные зубы, и слизистой оболочке вокруг имплантов. Клинические исследования, образцы биопленки и биопсия были получены как на ранних, так и на более поздних стадиях воспалительного поражения.
Через 3 недели наблюдалось обильное накопление биопленки, и в десне и слизистой оболочки были выявили клинические признаки воспаления. Гистология показала воспалительный клеточный инфильтрат в пределах соединительной ткани, который был обнаружен в краевой части мягких тканей, непосредственно прилегающий к барьерному эпителию в случае имплантов и к соединительному эпителию в случае естественных зубов. Напротив, после более длительного периода (90 дней) скопления биопленки, в случае периимплантационного мукозита в очаге содержалось меньшее количество фибробластов, чем в десневом образце, а площадь, занимаемая воспалительным инфильтратом была выше при повреждениях в области имплантов, чем при гингивите, хотя он не выходил за рамки барьерного эпителия.
Ericsson et al., в экспериментальном исследовании на собаках, получил биопсию слизистой оболочки после 9 месяцев накопления биопленки и показал воспалительный инфильтрат, расположенный в краевой части. В другом экспериментальном исследовании с длительно существующими поражениями в области трех систем имплантов были обнаружены связанные с биопленкой (в течение 5 месяцев) поражения. Результаты этого исследования подтвердили, что размер и апикальное удлинение воспалительного инфильтрата не выходит за пределы барьерного эпителия для всех трех систем имплантов.
Исследования с участием людей
Экспериментальные исследования с участием людей оценили ответ на 3 недельное накопление биопленки, соответствующее временным рамкам экспериментального гингивита Löe et al., где обратимость воспалительного поражения вокруг зубов имела место после восстановления контроля над биопленкой через 3 недели. Есть исследования, в которых сообщается о наблюдении за биопсийным материалом слизистой оболочки человека, полученным в результате длительного текущего поражения, вызванного биопленкой.
Gualini et al. описал иммуногистохимические особенности периимплантационного мукозита, полученного от 10 субъектов с частичным отсутствием зубов и установленными имплантами в течение от 2 до 5 лет.
Клинически степень гиперемии и отечности воспаленных тканей были разнообразны; тем не менее, все участки кровоточили при легком зондировании. Во всех биоптатах гистологические образцы показали небольшой и четко определенный воспалительный инфильтрат в соединительной ткани, прилегающий к барьерному эпителию.
Поражения включали 7,3% Т-клеток (CD3-положительные) и 4,1% В-клеток (CD19-положительный). Эластазоположительные полиморфноядерные нейтрофилы (ПМН) отмечались в барьерном эпителии и в некоторых участках соединительной ткани, непосредственно сбоку от барьерного эпителия. Площадь воспалительных поражений соответствовала до 0,36 мм2, что значительно превышает размер поражений, наблюдаемых в экспериментальном краткосрочном (3-недельном) мукозите в работе Zitzmann et al. и гистологических образцах,взятых в основном из клинически здоровых участков. Эти исследования подтвердили результаты Seymour et al., который также оценивал образцы у девяти испытуемых с многолетним мукозитом и обнаружил увеличение размера воспалительного поражения по сравнению с клинически здоровыми участкамти.
Перимплантационныймукозит может существовать в течение обширных временных интервалов без прогрессирования в периимплантит. Преобразование мукозита в периимплантит в экспериментальных моделях на людях затруднено по очевидным этическим соображениям.
Однако при продольном исследовании было показано, что у пациентов с диагнозом мукозит, у которых отсутствовала приверженность к поддерживающей терапии в области имплантов, в цлом чаще в течение 5 лет развивался периимплантит. Следовательно, следует учитывать участки с мукозитом при оценку повышенного риска развития периимплантита.
Факторы риска развития периимплантационного мукозита
На предыдущем Всемирном конгрессе, посвященном вопросам пародонтологии сам термин «фактор риска» был определен как «экологический, поведенческий или биологический фактор, присутствующий в определенном временном интервале, обычно изучается в продольных исследованиях, при наличии которого прямо увеличивает вероятность заболевания, а при его отсутствии или устранении эта вероятность уменьшается». Для выявления истинных факторов риска, как правило, необходимы проспективные исследования.
Большинство доступных исследований являются перекрестными или ретроспективными и, следовательно, в настоящем обзоре термин «риск» означает связь с развитием мукозита или каким-либо индикатором заболевания.
Общие показатели / факторы риска развития мукозита
Были изучены факторы, которые могут влиять на восприимчивость организма хозяина к мукозиту, вызванному биопленкой. Курение сигарет было идентифицировано как индикатор риска для мукозита в трех работах. Также имеются данные по лучевой терапии как факторе риска для мукозита. Имеются некоторые доказательства в отношении и сахарного диабета. Показано, что плохо контролируемый сахарный диабет (HbA1c>10,1) был связан с увеличением показателей кровоточивости в области имплантатов.
В то время как связь сердечно-сосудистых нарушений с риском развития преиимплантита была показана, не было доказательств ассоциации этих состояний с мукозитом. Máximo и соавт. сообщили, что присутствует значимая, но слабая корреляция (r = 0,44, тест Pearson χ2) между развитием мукозита и увеличением времени нагрузки имплантата. Однако, это исследование не учитывало сопутствующих факторов, и данная ассоциация, возможно, была связана с увеличением времени функционирования без регулярного удаления биопленки.
Аналогичным образом, в недавнем исследовании, проведенном с участием 193 пациентов с функционирующими имплантами не менее 12 месяцев (диапазон от 1 до 9 лет), была обнаружена ассоциация с возрастом и временем функционировании протеза. Однако, четкого различие между мукозитом и периимплантитом не было описано. Ferreira et a lтакже сообщил об ассоциации мукозита с системными заболеваниями. Однако под системными заболеваниями понималась целая группа состояний, «сахарный диабет, гормональные изменения, менопауза, химиотерапия, изменения щитовидной железы, проблемы с сердцем и алкоголизм», поэтому результаты исследования трудно интерпретировать.
Основные местные факторы риска
Гигиена полости рта
Результаты клинических исследований четко показали, что скопление биопленки связано с развитием периимплантационного мукозита вокруг интегрированных имплантов. Ferreira et al. сообщил об 212 пациентах, имеющих в полости рта три разных системы имплантов, у которых был диагностирован мукозит. Все импланты функционировали в течение периода от 6 месяцев до 5 лет. Был зафиксирован модифицированный индекс зубной бляшки, а общий уровень гигиены полости рта был определен как хороший (средний балл ≤1), низкий (средний балл> 1 и <2) и очень низкий (средний балл ≥2). Авторы сообщили о значительной связи между оценкой зубного налета и мукозитом. Распространенность мукозита была зарегистрирована на уровне 64,6%. Результаты другого исследования с участием 218 пациентов с 999 имплантами при их функционировании в течение периода от 9 до 14 лет, показали, что уровень зубного налета был значительно связаны с наличием мукозита у пациентов.
Регулярный контроль биопленки следует считать стандартом ухода и одновременно лечением при наличии преиимплантационного мукозита, который проводится либо пациентом самостоятельно или врачом-специалистом.
Наличие или отсутствие поддерживающей терапии в области имплантов (SIT)
Среди пациентов, не придерживающихся регулярной поддерживающей терапии (SIT), мукозит, как сообщалось, является распространенной проблемой в 48% случаев в течение периода наблюдения от 9 до 14 лет. И наоборот, результаты другого когортного исследования с 5-летним наблюдением показали, что имплантаты, установленные у пациентов с контролируемым пародонтальными состояниями и соблюдением программы SIT дают 20% распространенность мукозита. В этом исследовании, при постановке диагноза перииплантационный мукозит, все импланты за исключением одного из них были успешно обработаны в соответствии с анти-инфекционным протоколом. Результаты 3-месячного рандомизированного плацебо-контролируемого клинического исследования показали, что механическая обработка с или без местного применения геля на основе хлоргексидина в сочетании с оптимальным самоконтролем биопленки полностью устраняет кровоточивость при исследовании в области 38% имплантатов с диагнозом мукозит. У пациентов с частичным отсутствием зубов и наличием мукозита в сочетании с отсутствием приверженности к SIT в большем проценте случаев приводит к периимплантиту во время 5-летнего наблюдения. Результаты этого исследования показали заболеваемость периимплантитом в 18,0% в группе пациентов с SIT и в 43,9% в группе без SIT соответственно в течение 5 –летнего наблюдения. Регрессивный анализ показал, что отсутствие SIT в общей массе пациентов был значительно связан с началом периимплантитом с коэффициентом вероятности 5,92. Следовательно, терапию периимплантационного мукозита следует считать профилактикой периимплантита.
Материалы и характеристики поверхности компонентов имплантов
Доказательств влияния шероховатости поверхности имплантата на частоту мукозитов в области импланта встречается немного. 12-месячный сравнительный анализ у пациентов, у которых установлены обработанные титановые абатменты (Ra = 0,2 мкм) и полированные керамические абатменты (Ra = 0,06 мкм) показали, что дальнейшее уменьшение шероховатости поверхности не оказывает влияния на показатели кровоточивости при зондировании (BOP). Исследование на людях установило связь между изменяющейся шероховатостью поверхности абатмента и опорными и ранним воспалительным ответом слизистой оболочки вокруг имплантов. Хотя статистически значимое различие наблюдалось между пациентами в отношении накопления биопленки на поверхности абатмента и скоплением воспалительных клеток, не наблюдалось никакой ассоциации между воспалительным ответом и шероховатостью поверхности абатмента в течение 4 недельного наблюдения.
Сравнивая импланты и абатменты из титана, было выявлено, что больше полезных свойств с точки зрения биосовместимости имеется у имплантатов и абатментов из диоксида циркония (ZrO2). Следует, однако, отметить, что нет клинически значимых различий в показателях BOP между этими материала, а в некоторых случаях более высокий BOP были зарегистрированы около ZrO2 конструкций по сравнению с титановыми абатментами.
Дизайн протеза на имплантах
Возможность удаления биопленки вокруг протезов, опирающихся на импланты, играет важную роль в предотвращении периимплантита. Имплантаты с надслизистой частью дают значительное снижение глубины зондирования после лечения мукозита по сравнению с теми, которые имеют только подслизистую части. Этот вывод подтверждает предыдущие наблюдения о связи между восстановлением поддесневых частей на естественных зубах и воспаления пародонта, а также потере прикрепления.
Результаты клинического ретроспективного исследования показали наличие больших цифр имплантов с диагнозом периимплантит по причине недостаточного контроля биопленки или отсутствием доступности для гигиены полости рта, в то время как периимплантит редко обнаруживался на участках, где был контроль над биопленкой доступность гигиены не была нарушена.
Следовательно, инструкции и рекомендации по гигиене полости рта должны индивидуально адаптироваться к пациентам, получающим лечение по средствам установки дентальных имплантов, потому что мукозит можно считать предшественником периимплантита. Кроме того, по возможности, маргинальный край протеза, опирающегося на импланты следует размещать на уровне или выше слизистой оболочки для облегчения доступа и контроля биопленки.
Конструкции на имплантах, препятствующие доступу для удаления биопленки следует корректировать или заменить другими протезами.
Размеры кератинизированной слизистой оболочки в области имплантов
Влияние размеров кератинизированной слизистой оболочки в области имплантов как индикатор риска для развития мукозита был изучен в нескольких исследования на людях. Хотя в некоторых исследованиях сообщалось о более высоких показателях мукозита в области имплантов, у которых отмечалась нехватка или неадекватная ширина (менее 2 мм) кератинизированной десны , в других такой связи не было выявлено. В целом, доказательства наличия или минимальной ширины кератинизированной слизистой оболочки вокруг имплантатов для поддержания здоровья и стабильности мягких тканей довольно спорны. В клинических ситуациях при адекватной гигиене полости рта, пластика мягкими тканями при их дефиците, не является обязательной.
Избыточный цемент
Излишний цемент связан с клиническими признаками периимплантационного мукозита. Пациенты, у которых имеется одиночная коронка с избытком цемента проявляются больше признаков мукозита по сравнению с теми, у которых такие же коронки без избытка цемента. Кроме того, мукозит преобладал у пациентов с протезами, зафиксированными на цемент по сравнению с теми, у кого была выполнена цементо-винтовая фиксация.
Поэтому, чтобы избежать избытка цемента, края конструкции должны располагаться на уровне или над слизистой оболочкой или реставрации следует фиксировать на индивидуальные абатменты, обеспечивающие надлежащее удаление цемента.
Сходства и различия между факторами риска заболеваний пародонта и периимплантационным мукозитом
В недавнем систематическом обзоре обобщены потенциальные показатели риска в отношении развития мукозита, выделены следующие индикаторы: накопление биопленки и курение. Кроме того, исследования показали, что оценка уровня зубного налета была индикатором риска для развития мукозита, но являлась дозо-зависимой величиной. Данные, полученные за период 2009-2012 из «Обзора состояния здоровья и питания» (NHANES), определили курение сигарет как модифицирующий фактор риска для всех степеней тяжести пародонтита. Неконтролируемый диабет, мужской пол и возраста также были определены как факторы риска для патологий пародонта. Таким образом, определенно присутствуют сходства в показателях факторов риска для мукозита и пародонтита, хотя по-прежнему имеется недостаток информации, касающейся индикаторов риска для мукозита.
Состояние мукозита, несвязанное с биопленкой
Существуют заболевания слизистой оболочки полости рта, такие как красный плоский лишай (КПЛ) отрицательно влияющие на способность эпителия прикрепляться к поверхности титана. Следовательно, можно предположить, что пораженная слизистая оболочка в области имплантов при таких условиях также будет реагировать иначе, чем здоровая слизистая на бактериальную инфекцию, приводящей к более быстрому возникновению проблем с мягкими тканями вокруг имплантов. Распространенность мукозита оценивали у пациентов с диагнозом красный плоский лишай по сравнению с контрольными пациентами. Результаты показали, что наличие КПЛ не связано с более высокой распространенностью мукозита. Эти результаты были подтверждены в другом исследовании, не сообщалось о значительных различиях в распространенности мукозита у пациентов с имплантами и диагностированным КПЛ или без него. Однако у пациентов с диагнозом КПЛ в сочетании с десквамацией десны, значительно более высокая распространенность мукозита. Об этом сообщалось в исследовании Hernandez et al., возможно, такая ситуация быть связана с более высоким уровнем скопления зубной бляшки, связанное с данным стоматологическим состоянием само по себе или с обоими факторами.
Было высказано предположение, что некоторые пациенты могут страдать от аллергических реакций на материалы, такие как титан или сплавы титана, однако, данные по этому вопросу очень ограниченны.
Выводы
Периимплантационный мукозит — воспалительное поражение слизистой оболочки в области импланта при отсутствии прогрессирующей потери краевой костной массы.
Такой мукозит вызван прежде всего нарушением равновесия в системе хозяин-микрофлора в зоне имплантат-слизистая оболочка и является обратимым состоянием на уровне биомаркеров организма хозяина. Возврат к состоянию здоровья (клинически) в экспериментальных исследованиях при развитии мукозита может занять более 3 неделей при полном контроле биопленки. Факторы риска/индикаторы, связанные с развитием мукозита, включают скопление и рост биопленки, курение и лучевая терапия. Регулярная поддерживающая терапия в области имплантов с удалением биопленки является важной профилактической стратегией в отношении развития мукозита, а также препятствует прогрессированию мукозита к периимплантиту.
Обзор клинических исследований
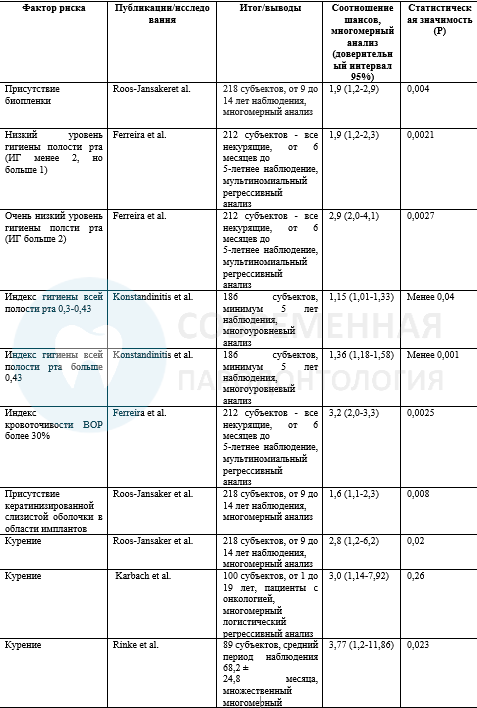
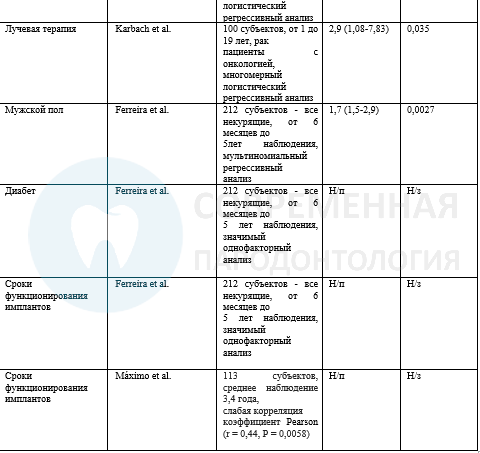
Перевод материала выполнен авторами «Современная пародонтология». Оригинал материала и список литературы находится по ссылке
