Конечная цель лечения пародонтита заключается не только в устранении воспаления и предотвращении прогрессирующей потери прикрепления, но и в регенерации всех утраченных тканей пародонта, включая альвеолярную кость, периодонтальную связку и цемент.
Традиционно процедуры, направленные на восстановление утраченных тканей, требуют хирургического подхода для доступа к костным дефектам. За последние 50 лет хирургические техники значительно развились благодаря улучшению понимания биологических принципов заживления ран. Современные хирургические методы включают использование микрохирургических инструментов и минимально инвазивные подходы, которые позволяют обеспечить стабильность кровяного сгустка, необходимого для заживления раны и достижения регенеративного результата.
Хотя в литературе продолжают описывать новые хирургические методы, общей целью остается сохранение межзубных сосочков. Однако следует признать, что нехирургические методы, исключающие разрезы и формирование лоскутов, не создают оптимальных условий для мягких тканей для поддержания регенеративных процессов. Это привело к появлению исследований, посвященных минимально инвазивной нехирургической терапии (MINST) как способу лечения внутрикостных дефектов без обязательного хирургического вмешательства. На данный момент нет стандартизированного определения MINST. Однако его можно охарактеризовать как нехирургический подход в пародонтологии, направленный на удаление биопленки с минимальной травмой мягких тканей и без утраты структур зуба, что способствует стабилизации кровяного сгустка для оптимального заживления раны.
Первое рандомизированное контролируемое исследование, продемонстрировавшее эффективность MINST, сравнивало нехирургический и хирургический подходы при лечении внутрикостных дефектов. В нехирургическом методе использовались ультразвуковые аппараты с тонкими наконечниками и мини-кюреты, минимально травмирующие мягкие ткани. Хирургический метод включал минимально инвазивную технику без применения биоматериалов. Через 6 месяцев различий в клинических показателях между двумя группами не выявили, но нехирургический метод позволил сократить время лечения.
Еще одно ретроспективное исследование, проведенное в частной практике на протяжении 5 лет, подтвердило эффективность MINST для устранения внутрикостных дефектов с рентгенологическим подтверждением регенерации костной ткани и положительными результатами.
По мере увеличения популярности MINST становится актуальным использование биологических препаратов для оптимизации результатов аналогично хирургическим методам. Биологические препараты — это агенты с биологической активностью, которые вводятся для усиления регенеративного эффекта. Недавние исследования сосредоточены на изучении биологических препаратов в качестве средства для модификации процессов заживления ран вместо простого использования местной антимикробной терапии, направленной преимущественно на контроль биопленки.
Производные эмалевого матрикса (EMD) являются перспективным вариантом благодаря хорошо задокументированной эффективности в хирургической регенерации тканей пародонта. Они способствуют прикреплению, миграции и пролиферации мезенхимальных клеток, регулируют факторы роста и стимулируют активность фибробластов и остеобластов. Традиционно EMD применяют на 3 этапе лечения пародонтита, особенно при наличии внутрикостных дефектов и дефектов фуркации II класса.
В данном клиническом случае речь пойдет о минимально инвазивном нехирургическом подходе при лечении остаточных пародонтальных карманов после 1 и 2 шагов терапии с использованием производных эмалевого матрикса для стимуляции регенерации.
Описание клинического случая
Пациентка, 48 лет, была направлена её стоматологом в специализированную стоматологическую клинику из-за опасений по поводу прогрессирующей потери костной ткани. После клинического и рентгенологического обследования ей поставили диагноз: генерализованный пародонтит IV стадии, степень С, нестабильный, без выявленных факторов риска.
После начального курса нехирургического лечения, включавшего обучение гигиене полости рта, наддесневую профессиональную механическую обработку корней (PMPR) и поддесневую PMPR участков с глубиной карманов ≥4мм и кровоточивостью при зондировании ≥5мм, пациентке провели повторную оценку паростатуса через 3 месяца. Остаточные участки с глубиной карманов были дополнительно обработаны нехирургическим методом, и ещё один осмотр был проведен спустя 3 месяца.
На этом этапе был выявлен карман в интерпроксимальной зоне глубиной 8мм на медиальной поверхности зуба 3.2 с признаками нагноения при зондировании. Средне-вестибулярные и средне-язычные поверхности зуба имели карманы глубиной не более 3мм. Рентгенография подтвердила 80% потерю костной ткани и наличие внутрикостного дефекта на медиальной поверхности зуба 3.2.
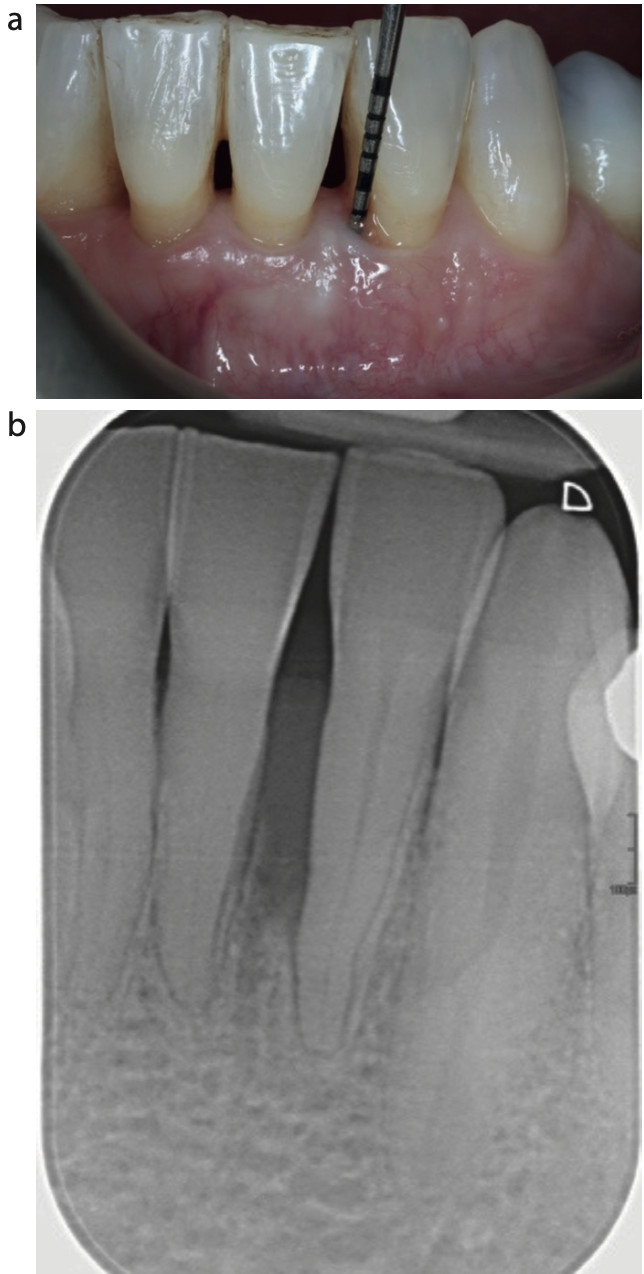
Фото 1. (a) до лечения: глубина кармана 8мм после двух этапов стандартной нехирургической терапии, (b) рентгенограмма периапикальной зоны, показывающая внутрикостный дефект с утратой 80% костной ткани в области 3.2
После обсуждения с пациенткой были предложены следующие варианты лечения:
- поддесневая PMPR с локальной доставкой антимикробных препаратов;
- поддесневая PMPR с использованием производного эмалевого матрикса (Emdogain, Institut Straumann AG, Швейцария);
- регенеративная пародонтологическая хирургия с дополнительным использованием биоматериалов.
Пациентка выбрала нехирургическое лечение с применением производного эмалевого матрикса. Терапия проводилась в соответствии с принципами минимально инвазивных нехирургических методик. Использовались тонкие ультразвуковые аппараты (Cavitron, Dentsply Sirona, Великобритания), мини-кюреты (LM Dental, Финляндия) и методы атравматичного воздействия на мягкие ткани.
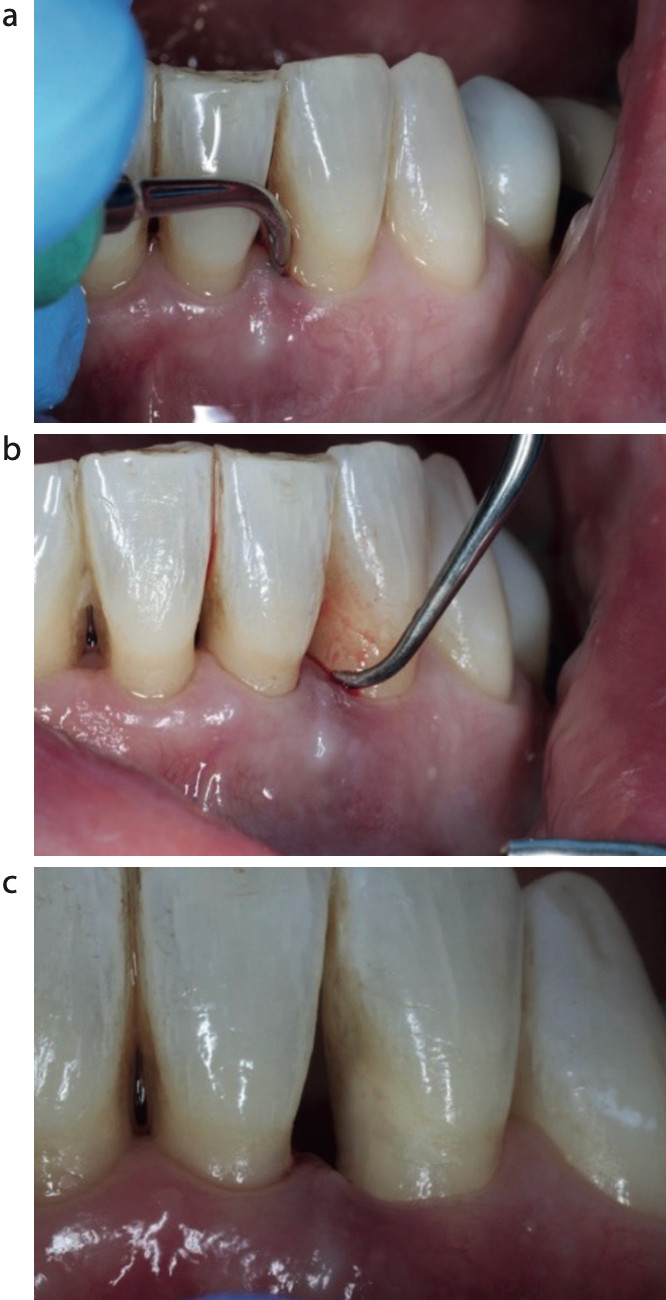
Фото 2. Фотографии в процессе лечения (a) ультразвуковая обработка, (b) использование микро-кюрет, (c) минимальная травма мягких тканей сразу после операции
Местная анестезия проводилась вестибулярно инфильтрациями артикаина 4% с адреналином 1:100 000. Применялось увеличение (x3,5 Omnioptics, Orascoptic). После тщательной обработки корневой поверхности и минимальной травмы мягких тканей, субгингивально был нанесён Эмдогейн. Предварительно корневой кондиционер с 24%-ным ЭДТА (PrefGel, Straumann) был оставлен в кармане на 2 минуты, после чего карман промыли стерильным физиологическим раствором. Для контроля влажности использовался суперфлосс (Oral-B), чтобы обеспечить контакт Эмдогейна с корнем до попадания крови. Гемостаз был достигнут перед тем, как пациент покинул кресло, кровяной сгусток оставался стабильным при отсутствии активного кровотечения. Антибиотики после лечения не назначались.
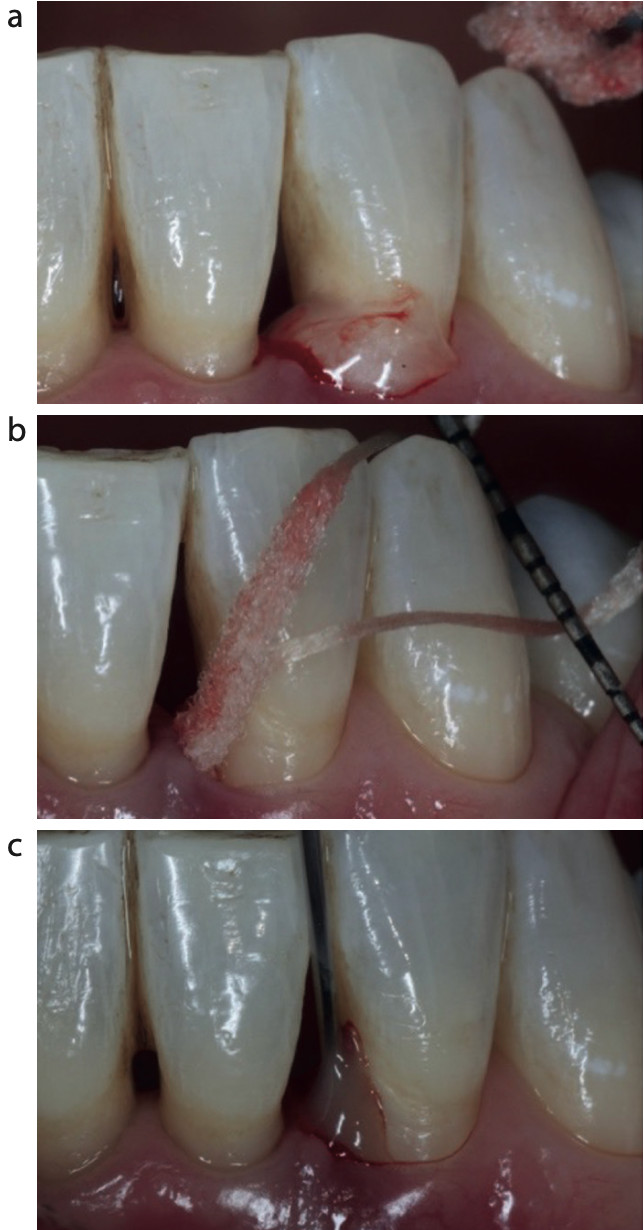
Фото 3. Применение производного эмалевого матрикса. (a) 24%-ный ЭДТА (PrefGel), (b) использование Superfloss для контроля влажности, (c) нанесение Emdogain с помощью тонкой канюли
Пациентке предоставили индивидуальные рекомендации по гигиене полости рта, включая использование межзубных щеток и электрической зубной щётки. Через 3 месяца ей провели поддерживающую пародонтологическую терапию, которая включала наддесневую PMPR и повторное обучение гигиене. Зондирование данного кармана в этот визит не проводилось, чтобы позволить процессам заживления продолжиться.
Через 6 месяцев специалист-пародонтолог повторно осмотрел пациентку. Исследования включали 6-точечное зондирование карманов и рентгенографию. Выявлено уменьшение глубины кармана в области зуба 3.2 с 8мм до 3мм с увеличением рецессии на 1мм, что обеспечило увеличение клинического прикрепления на 4мм. Рентгенография показала значительное заполнение костного дефекта и признаки формирования кортикальной пластинки, свидетельствующие о стабильности.
Пациентка была включена в программу поддерживающего лечения с осмотрами каждые 3 месяца и ежегодным контрольным обследованием.
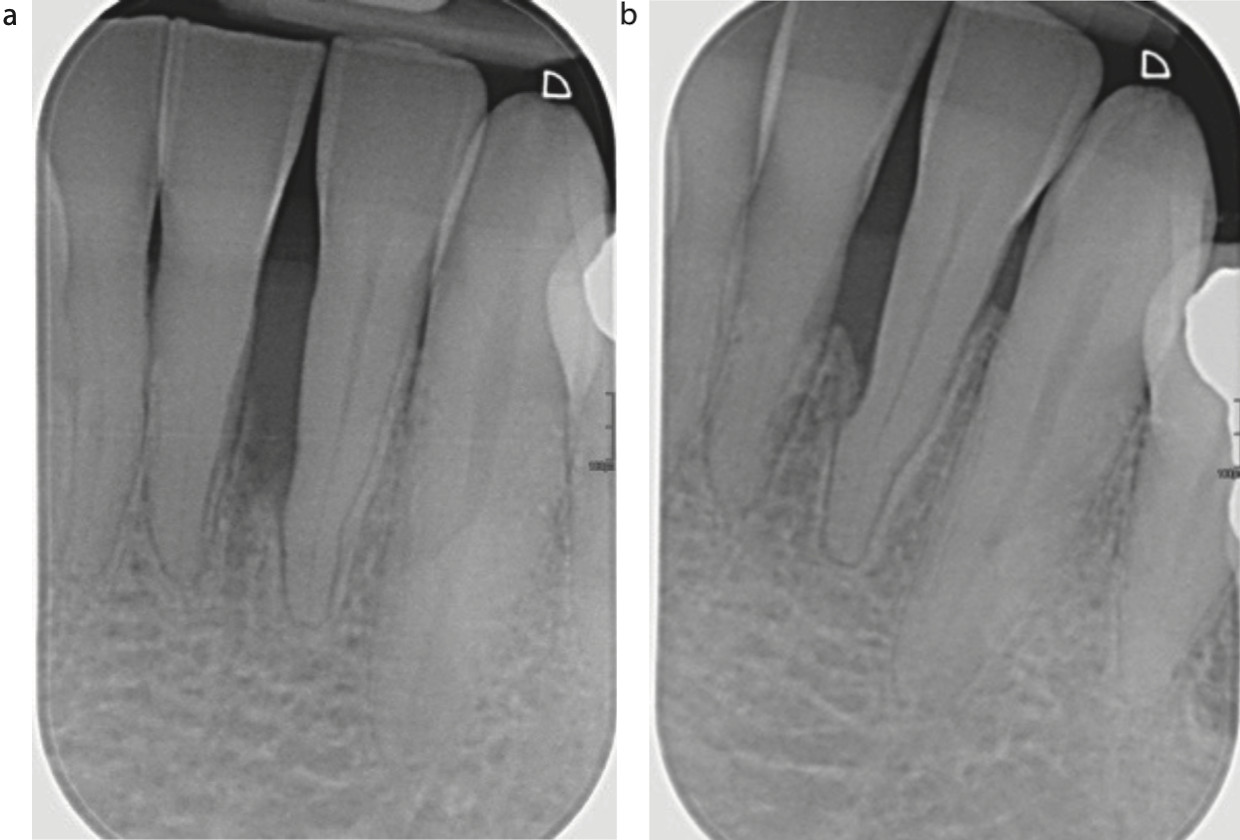
Фото 4. (a) Рентгенограммы до лечения и (b) через 6 месяцев после лечения, показывающие признаки заполнения костного дефекта и целостность компактной пластинки
Обсуждение
Первый случай успешной хирургической регенерации тканей на человеческом зубе был описан в 1982 году. С тех пор дизайн лоскутов и подходы к хирургическому лечению продолжали эволюционировать. Современные методы ориентированы на минимизацию травматизации мягких тканей и максимально малоинвазивный доступ. Эти изменения основаны на понимании, что стабильная рана с первичным заживлением играет ключевую роль в регенеративных процессах.
В связи с этим минимально инвазивная нехирургическая терапия (MINST) набирает популярность в клинической практике. Однако на сегодняшний день общепринятый протокол MINST еще не разработан. Исследования предлагают основные концепции, лежащие в основе данной методики:
- тщательное удаление биопленки с поверхности корня вплоть до дна пародонтального кармана;
- использование мини-кюрет и ультразвуковых аппаратов с тонкими насадками;
- применение увеличения в ходе манипуляций;
- минимизация травматизации мягких тканей для сохранения их стабильности.
В представленном случае использовалась местная анестезия с вазоконстриктором, несмотря на то, что некоторые протоколы MINST избегают этого, чтобы способствовать формированию стабильного кровяного сгустка. На сегодняшний день нет доказательств, что использование анестетиков без вазоконстрикторов дает лучшие результаты при данной процедуре.
Применение производных эмалевого матрикса (EMD) в сочетании с нехирургической терапией не является новой концепцией. Впервые это было изучено в 2003 году, однако ранние исследования не показали значительных преимуществ EMD в снижении глубины пародонтальных карманов (PPD) и увеличении клинического уровня прикрепления (CAL). Это могло быть связано с тем, что техника обработки корня тогда не предусматривала атравматичное воздействие на мягкие ткани, что противоречит современным принципам MINST.
В недавнем систематическом обзоре и метаанализе было установлено, что при оценке результатов снижения глубины кармана (PPD) и прироста клинического уровня прикрепления (CAL) добавление EMD не дало преимущества по сравнению с одной лишь нехирургической терапией. Эти результаты следует интерпретировать с осторожностью и не рассматривать как доказательство отсутствия потенциала у этих материалов. Данный первый метаанализ включал только четыре исследования, которые при детальном рассмотрении показали различия в применении EMD: в некоторых исследованиях биологический материал использовался на этапе 2, а в других — на этапе 3. Как показано в этом клиническом случае, для корректного и эффективного применения материала требуется адекватный контроль влажности/кровотечения. Таким образом, более практичным может быть использование EMD на этапе 3 терапии, когда воспаление уменьшилось, качество тканей начало улучшаться, и если остаются остаточные карманы.
Необходимо также учитывать уменьшение PPD и прирост CAL в качестве основных критериев эффективности, поскольку фактор, определяющий клиническое решение и необходимость дальнейшего вмешательства (например, хирургического), — это достижение закрытия кармана (PPD ≤4мм без BOP). Недавнее многоцентровое рандомизированное контролируемое исследование изучало закрытие карманов после применения EMD совместно с нехирургической терапией на этапе 3 (то есть после завершения первоначальной терапии и при наличии остаточных карманов) по сравнению с контрольной группой, получавшей повторное нехирургическое лечение. Через 12 месяцев в 80% случаев в тестовой группе наблюдалось закрытие карманов, в то время как в контрольной группе — только в 42%. Это позволяет предположить, что EMD может играть роль в лечении остаточных карманов до принятия решения о хирургическом вмешательстве.
В последнее время, в контексте применения регенеративных методов лечения, начали использовать составные показатели результатов (закрытие кармана и прирост CAL ≥3мм), впервые описанные Trombelli и коллегами для хирургических вмешательств, и сейчас они применяются в исследованиях, основанных на MINST. Недавнее рандомизированное контролируемое исследование показало, что больше участков, обработанных с использованием EMD, достигли данных составных показателей по сравнению с теми, которые получали только нехирургическую терапию.
Ограничения, связанные с единичным клиническим случаем, необходимо учитывать, особенно отсутствие контрольной группы, которая позволила бы сравнить полученные результаты с другими вариантами лечения, такими как исключительно минимально инвазивная нехирургическая терапия или минимально инвазивный хирургический подход с использованием или без использования биоматериалов, которые могут дать аналогичные или лучшие регенеративные результаты.

Заключение
Учитывая ограничения, присущие описанию случаев, данный случай демонстрирует потенциал использования производных эмалевого матрикса в качестве дополнения к минимально инвазивной нехирургической терапии для лечения внутрикостных дефектов при наличии остаточных карманов после второго этапа терапии. Будущие исследования в формате рандомизированных контролируемых испытаний, а также сбор данных о результатах лечения пациентов могут подтвердить эффективность данного подхода. Это позволит широкой группе специалистов применять данный метод и, возможно, избежать хирургических вмешательств.
По материалам Devan S Raindi, Paul Weston, Iain Chapple «Case Report: Non-surgical Regeneration with Adjunctive Enamel Matrix Derivative», 2024
